资料显示:a.Na2S2O3、BaS2O3、BaS均易溶于水。
b.SO2、Na2S、Na2CO3反应可生成Na2S2O3。
某化学小组据此进行了制备硫代硫酸钠(Na2S2O3)的探究:
实验制备装置如下图所示(省略夹持装置):
回答问题:
(1)仪器a的名称是 。
(2)装置A中发生反应的化学方程式是 。
(3)装置B的作用之一是观察SO2的生成速率。
①B中最好盛装的液体是 。
a.蒸馏水
b.饱和Na2SO3溶液
c.饱和NaHSO3溶液
d.饱和NaHCO3溶液
②如使SO2缓慢进入烧瓶C,正确的操作是_________。
(4)在装置C中生成Na2S2O3。
①完成反应方程式: SO2 + Na2S + Na2CO3 = Na2S2O3 +
②反应开始先使A中发生反应一会儿,再使C中反应发生,其原因是 。
③结束反应后,取C中溶液,经________、结晶、过滤、洗涤、干燥、得到Na2S2O3·5H2O。
(5)完成对所得产品的检测的实验:
| 推测 |
操作和现象 |
结论 |
| 杂质中的正盐成分可能有: Na2S Na2CO3 Na2SO4 |
①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生。 ④向滤液滴加2滴淀粉溶液,再逐滴加0.100 0 mol·L-1碘的标准溶液,至溶液呈紫色不再褪去,消耗碘的标准溶液体积为18.10mL。 |
产品杂质中: 一定含有 , 可能含有 , 一定不含有 。 操作④发生的反应是: 2S2O32-+I2===S4O  +2I- +2I-产品纯度: 。 |
工业和交通运输业的迅速发展,城市人口的高度集中,机动车数量的日益增多,人类向大气中大量排放烟尘和有害气体等,对大气造成了严重的污染。启东市近期一次的“空气质量日报”显示,启东的空气已受到一定程度的污染。一研究性学习小组对启东市的空气污染情况进行了下列研究。
⑴小组一同学初步分析得出,启东市空气污染的主要原因可能有如下三种:
A、使用石油液化气 B、燃烧含硫煤 C、粉尘污染
另一同学认为还有一个不可排除的原因是:D:
研究性学习小组就造成启东市空气污染的最主要原因调查了本市100名市民和100位环保部门人士。调查结果如下图所示:
空气污染原因调查人数分布图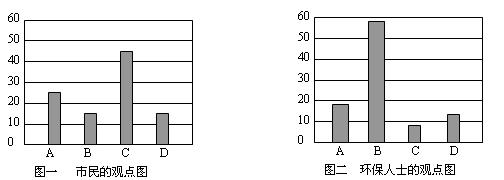
从市民和环保人士的不同观点上分析,你认为造成启东市空气污染的主要有害成分是
(用化学式表示)
⑵空气污染形成酸雨。研究性学习小组对启东市的雨水进行了采样和分析,刚采集时测得PH为4.82,放在烧杯中经2小时后,再次测得PH为4.68,较长一段时间后发现PH不再变化,对此,你的合理解释是
⑶研究性学习小组取相当于标准状况下的空气1.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤,干燥,称得其质量为0.233g,进行这一实验的目的是,通过计算得到的结论是(以定量描述)
⑷该小组提出下列措施以减少空气污染主要有害成分排放量,你认为合理的是
(填序号)
①用天然气代替煤炭作民用燃料②改进燃烧技术,提高煤的燃烧效率
③工厂生产时将燃煤锅炉的烟囱造得更高④燃煤中加入适量石灰石后使用
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: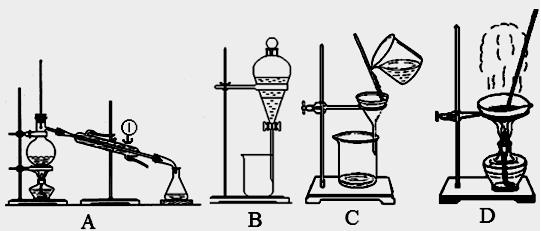
(1)从氯化钾溶液中得到氯化钾固体,选择装置(填代表装置图的字母,下同);除去自来水中的 Cl-等杂质,选择装置。
Cl-等杂质,选择装置。
(2)从碘水中分离出I2,选择装置,该分离方法的名称为。
(3)装置A中①的名称是,进水的方向是。
装置B在分液时为使液体顺利下滴,应进行的具体操作是
。
用18.4mol/L的浓硫酸配制100mL浓度为1mol/L的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、、。
(2)其操作步骤可分解为以下几步:
A.用量筒量取mL浓硫酸,缓缓注入装有约50mL蒸馏水的烧杯里,并用玻璃棒搅拌
B.用约30mL蒸馏水分三次洗涤烧杯和玻璃棒,将每次的洗液都倒入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流容量瓶里
D.检查100mL容量瓶,是否漏水
E.将蒸馏水直接加入容量瓶,至液面接近刻度线
F.盖紧瓶塞,反复颠倒振荡,摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到液面最低点恰好与刻线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
()→()→()→()→()→()→()。
③进行A步操作时,选用量筒的规格是
A.10mL B.50mL C.100mL D.1000mL
④如果对装有浓硫酸的量筒仰视读数,配制的稀硫酸浓度将(填“偏高”、“偏低”、“无影响”)
⑤A步骤操作完成时,必须后,才能进行后面的操作。
松花蛋于明朝初年问世。其腌制配方有多种,但主要配料为生石灰(CaO)、纯碱(Na2CO3)和食盐(NaCl)。将一定比例的配料用水和粘土调制成糊状,敷于蛋上,密封保存,数日后即可食用。
(1)腌制皮蛋的配料用水调制时,主要反应的化学方程式为(不考虑粘土中物质可能参与的反应)
。
(2)松花蛋外的糊状物经水溶解、过滤,滤液中肯定大量含有的溶质为和,可能含有的物质为Ca(OH)2或Na2CO3。
(3)某同学设计如下表所示的实验方案,探究(2)所得滤液中可能含有的物质是否存在,请你帮他完善实验方案。
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量滤液,滴加适量K2CO3溶液 |
滤液中含 |
|
| 滤液中无 |
||
| ②另取少量滤液,滴加 |
滤液中含 |
|
| 滤液中无 |
问题讨论:在什么情况下不必做实验②就可以得出滤液中有无Na2CO3的结论?
海带中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:(已知:Cl2 + 2KI =" 2KCl" + I2)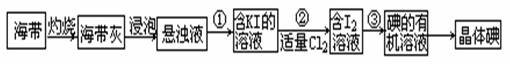
(1)提取碘的流程中:步骤①需要的主要仪器是,步骤③需要的主要仪器是(填序号)
(2)写出步骤②中涉及的有关离子反应方程式。
(3)提取碘的过程中,可供选择的有机试剂有。
| A.四氯化碳 | B.醋酸 | C.酒精 | D.苯 |