下列解释事实的方程式不正确的是
A.测0.01mol/L的醋酸的pH为5:CH3COOH CH3COO- + H+ CH3COO- + H+ |
B.电解饱和食盐水,产生气体:2Cl- + 2H2O Cl2↑+2OH- + H2↑ Cl2↑+2OH- + H2↑ |
C.铁放在氧气中燃烧,产生黑色固体:4Fe +3O2 2Fe2O3 2Fe2O3 |
D.硫酸钙与碳酸钠溶液,产生白色沉淀:CaSO4(S)+CO32- CaCO3(S)+SO42- CaCO3(S)+SO42- |
如图表示外界条件(温度、压力)的变化对下列反应的影响:L(s)+G(g) 2R(g)ΔH>0。在图中Y轴是指
2R(g)ΔH>0。在图中Y轴是指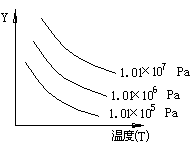
| A.平衡混合气中R的质量分数 | B.G的转化率 |
| C.平衡混合气中G的体积分数 | D.L的转化率 |
对可逆反应2A(s)+3B(g)  C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
C(g)+2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v(正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
| A.①② | B.③ | C.④ | D.④⑤ |
某温度下,密闭容器中发生反应aX(g)  bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
bY(g)+cZ(g),达到平衡后,保持温度不变,将容器的容积压缩到原来容积的一半,当达到新平衡时,物质Y和Z的浓度均是原来的1.8倍。则下列叙述正确的是
| A.可逆反应的化学计量数:a>b+c |
| B.压缩容器的容积时,v(正)增大,v(逆)减小 |
| C.达到新平衡时,物质X的转化率减小 |
| D.达到新平衡时,混合物中Z的质量分数增大 |
在给定的四种溶液中,加入以下各种离子后,各离子能在原溶液中大量共存的有
| A.滴加酚酞试液显红色的溶液:Fe2+、NH4+、Cl–、I– |
| B.水电离出来的c(H+)=10-13mol·L–1的溶液:K+、HCO3–、Br–、Ba2+ |
| C.在c(H+)=10-13 mol·L–1的溶液:K+、SO42–、Al3+、Cl– |
| D.PH=1的溶液:Cu2+、Na+、Mg2+、NO3– |
一定温度下反应N2+O2 2NO在密闭容器中进行,下列措施不改变化学反应速率的是
2NO在密闭容器中进行,下列措施不改变化学反应速率的是
| A.缩小体积使压强增大 | B.恒容,充入N2 |
| C.恒容,充入He | D.恒压,充入He |