中国首个空间实验室—“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,a、b、c、d均为Pt电极。下列说法正确的是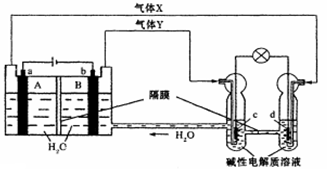
A、B区的OH-通过隔膜向a电极移动,A区pH增大
B、图中右管中的OH-通过隔膜向c电极移动,d电极上发生还原反应
C、c是正极,电极上的电极反应为: 2H++2e-=H2↑
D、当有1 mol电子转移时,b电极产生气体Y的体积为11.2 L
右图是元素周期表中短周期的一部分,X、Y、Z、W四种元素的原子核外最外层电子数之和等于Y、Z元素的原子序数之和。下列说法不正确的是
| X |
Y |
||
| Z |
W |
A.X元素形成的气态氢化物分子的空间结构是三角锥形
B.Z与Y元素形成的化合物熔点很高
C.W单质分子间作用力较大,加压时易液化
D.Z的最高价氧化物能溶于X的最高价氧化物的水化物中
几种短周期元素的原子半径及主要化合价见下表:
| 元素符号 |
X |
Y |
Z |
R |
T |
| 原子半径(nm) |
0.160 |
0.111 |
0.104 |
0.143 |
0.066 |
| 主要化合价 |
+2 |
+2 |
-2,+4,+6 |
+3 |
-2 |
根据表中信息,判断以下说法正确的是
A.单质与稀硫酸反应的速率快慢:R>Y>X
B.离子半径: X2+>T2-
C.元素最高价氧化物对应的水化物的碱性:Y > R >X
D.相同条件下,等物质的量的单质与氢气化合放出能量的多少:T>Z
已知,常温下,KSP (AgCl)=1.8×10-10 mol2·L-2,KSP(AgI)=8.3×10-17 mol2·L-2,下列叙述中,正确的是
| A.常温下,AgCl在饱和NaCl溶液中的KSP比在纯水中的KSP小 |
| B.向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 |
| C.将0.001 mol·L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 |
| D.向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) |
25℃时,水中存在电离平衡:H2O  H++OH- ΔH>0。下列叙述正确的是
H++OH- ΔH>0。下列叙述正确的是
| A.将水加热,Kw增大,pH不变 |
| B.向水中加入少量NaHSO4固体,c(H+)增大,Kw不变 |
| C.向水中加入少量NaOH固体,平衡逆向移动,c(OH-)降低 |
| D.向水中加入少量NH4Cl固体,平衡正向移动,c(OH-)增大 |
下列说法中,不正确的是
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成了一层致密的氧化膜
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤向蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性
| A.①③④⑤ | B.②③④ | C.①③④ | D.①②③④⑤ |