下列实验“操作和现象”与“结论”对应关系正确的是
| 选项 |
操作和现象 |
结论 |
| A |
CH4和Cl2混合于试管中光照,颜色逐渐褪去 |
二者发生了化合反应 |
| B |
微热滴有2滴酚酞的饱和NaHCO3溶液,溶液颜色加深 |
NaHCO3受热分解生成了Na2CO3 |
| C |
向淀粉溶液中加入20%的硫酸,加热几分钟,冷却后再加入银氨溶液,水浴,没有银镜生成 |
淀粉没发生水解 |
| D |
向装有Fe(NO3)2溶液的试管中加入稀硫酸,观察到试管口有红棕色气体产生 |
酸性环境下,NO3-被Fe2+还原为NO,NO遇氧气生成NO2 |
在CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,发现铁钉并无任何变化。根据上述现象,确定下面结论正确的是
| A.不溶物一定是Cu | B.不溶物一定含铜,但不一定含铁 |
| C.不溶物一定是Fe | D.溶液中一定含有Fe2+,但不一定含有Cu2+ |
有 Al2(SO4)3 ,FeSO4,CuCl2, NaOH四种溶液,将其两两反应,若有一种溶液滴入另两种溶液中均产生了白色沉淀,继续滴加该溶液,原白色沉淀或消失或发生颜色变化,则可推断这一种溶液是
| A.Al2(SO4)3 | B.FeSO4 | C.BaCl2 | D.NaOH |
对于某些离子的检验及结论正确的是
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32— |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42— |
| C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
常温下,在100ml 12mol·L—1的浓HNO3中加入足量的铁粉,最终产生标准状况下气体的体积为(不考虑NO2转化为N2O4)
| A.几乎无气体产生 | B.等于6.72L[来 |
| C.等于13.44L | D.介于6.72L至13.44L之间 |
下列反应的离子方程式书写正确的是
| A.硫酸铝溶液中加入过量氨水 Al3++3OH- = Al(OH)3¯ |
B.电解饱和食盐水 2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| C.钠与水的反应 Na+2H2O = Na++2OH- +H2↑ |
D.单质铜与稀硝酸反应 Cu + 2H++ 2NO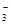 = Cu2+ + 2NO↑+H2O = Cu2+ + 2NO↑+H2O |