短周期元素X、Y、Z、W在周期表中的位置如图所示,其中W的氧化物是形成酸雨的主要物质之一。
| X |
|
|
|
| Z |
|
W |
Y |
(1)写出W的离子结构示意图: 。其单质与最高价氧化物对应的水化物反应的化学方程式是_________。
(2)已知:①X(s) + O2(g) =XO2(g) ΔH=-393.5 kJ·mol-1
②H2(g) + 1/2 O2(g) =H2O(g) ΔH=-242.0 kJ·mol-1
③XH4(g) + 2O2(g) =XO2(g) + 2H2O(g) ΔH=-802.0 kJ·mol-1
则XH4气体分解成氢气和X固体的热化学方程式为 。XH4分子空间构型是 ,其与Y的单质在光照时发生反应可以产生常用的有机溶剂,则该反应的类型是________。
(3)①XH4可与氧气构成燃料电池,若电解质溶液为KOH,则该燃料电池的负极电极反应式是______,电池的总反应方程式是____________。
②若以该电池产生的电能为电源,以石墨为电极电解500ml某浓度的CuSO4溶液,当电解完全,共产生Cu的质量是96g, CuSO4溶液溶液的浓度是_______。若甲烷燃料电池的能量利用率是75%,则会消耗标准状况下的甲烷的体积是_________。
(4)将X的最高价氧化物通入一定量的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,生成气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。
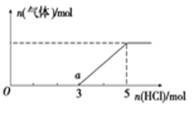
①O点溶液中所含溶质的化学式为____________。
②该溶液中溶质的物质的量是_______________。
向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式________________________;
(2)下列四种情况下,离子方程式与(1)相同的是_____________(填序号)
| A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量 |
| B.向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至Ba2+恰好完全沉淀 |
| C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性 |
| D.向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至过量 |
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用如图中的曲线表示是_______(填序号)
(4)向Ba(OH)2溶液中加入密度为1.165g/cm3的硫酸溶液,直到恰好完全反应为止,已知所生成的沉淀的质量等于加入的H2SO4溶液的质量,则硫酸溶液的浓度为_______mol/L。
pH=12的NaOH溶液100mL,要使它的pH=11。(体积变化忽略不计)
(1)如果加入蒸馏水,应加____________mL;
(2)如果加入pH=10的NaOH溶液,应加____________mL;
(3)如果加0.01 mol/L HCl,应加____________mL。
(1)将等质量的Zn粉分别投入:a:10mL0.1 mol•L-1HCl和b:10mL0.1 mol•L-1的醋酸中。
①若Zn不足量,则反应速率a___________b;(填“>”、“=”或“<”)
②若Zn过量,产生H2的量a__________b;(填“>”、“=”或“<”)
(2)将等质量的Zn粉分别投入pH=1体积均为10mL的a:盐酸 b:醋酸中。
①若Zn不足量,则反应速率a__________b;(填“>”、“=”或“<”)
②若Zn过量,产生H2的量a__________b;(填“>”、“=”或“<”)
已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有以下几种
①c(Cl-)>c(NH4+)>c(H+)>c(OH-)
②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
(1)上述关系一定不正确的是_______________(填序号);
(2)若溶液中只有一种溶质,则该溶质为__________,该溶液中离子浓度的大小关系为_______(填序号);
(3)若关系③正确,则溶液中溶质为_________;
(4)若四种离子浓度关系有c(NH4+)=c(Cl-),则该溶液显_________(填“酸性”、“碱性”、“中性”)。
(5)25℃,pH=a的盐酸VamL与pH=14-a的氨水VbmL混合,若溶液显中性,则Va__________Vb(填>、<、=、无法确定)。
用平衡移动原理分析外界条件对电离平衡的影响,如:以0.1 mol•L-1醋酸为例,对CH3COOH CH3COO-+H+进行分析:(填“增大”“减小”“不变”“正方向”“逆方向”)
CH3COO-+H+进行分析:(填“增大”“减小”“不变”“正方向”“逆方向”)
(1)当向该溶液中加水,则平衡向________方向移动;溶液的n(H+)_______;溶液的c(H+)_______;
(2)当向溶液中加入1 mol•L-1的醋酸时,平衡向_____方向移动;溶液的n(H+)_______;溶液的c(H+)_______。