在短周期元素中,A元素M电子层上有7个电子,C元素与A元素同主族,B元素与A元素位于同一周期,B元素的原子最外电子层只有1个电子。
(1)画出B元素的原子结构示意图______________。
(2)C、B两元素形成化合物的化学式是___________,其形成过程用电子式表示为______________。
(3)写出B的两种氧化物的电子式: 、 。
(4)比较A元素的氢化物与C元素的氢化物稳定性: (填化学式及“<、>或=”)原因为: 。
下面给出了四种有机物A、B、C、D的相关信息:
①烃A在所有的烃中含碳的质量分数最低
②烃B是一种植物生长调节剂,可用于催熟果实
③烃C在氧气中燃烧产生的氧炔焰常用来切割或焊接金属
④医疗上常用体积分数为75%的D溶液来消毒
据此回答有关问题:
(1)将A和Cl2混合充入一试管,密封后置于光亮处,一段时间后能看到试管内壁上出现的油状物不可能是__________(填编号)。
A.CH3Cl B.CH2Cl2 C.CHCl3 D.CCl4
(2)实验室制取B,常因温度过高而使乙醇和浓硫酸反应生成少量的SO2。某同学设计下列实验以确定上述混合气体中含有B和SO2。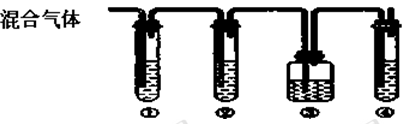
I.装置可盛放的试剂是:②: ④: (请将下列有关试剂的序号填入空格内)
A、品红 B、NaOH溶液 C、浓硫酸 D、酸性KMnO4溶液
Ⅱ.确定含有B的现象是。
(3)烃C的结构式为。
(4)D中加入冰醋酸、浓硫酸和少量H218O加热一段时间后,18O存在于
①存在于冰醋酸和水分子中②只存在于水分子中
③存在于D和冰醋酸分子中④存在于冰醋酸和D与醋酸形成的酯分子中
苹果酸是一种常见的有机酸,其结构简式为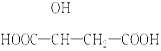 :
:
(1)苹果酸分子所含官能团的名称是 、。
(2)写出苹果酸与足量的钠反应的化学方程式:。
(3)写出苹果酸在浓硫酸加热下与乙酸反应的化学方程式 _____________________、
反应类型为。
(4) 1mol苹果酸与足量碳酸钠充分反应生成的气体在标准状况下体积最多为。
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义
(1)硫酸生产中,SO2催化氧化生成SO3; 2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题,
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题,
①2SO2(g)+O2(g) 2SO3(g)的△H0
2SO3(g)的△H0
(填“>”或“<”):若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”“向右”或“不”)
②若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1K2;反应进行到状态D时, 
 (填“>”“<”或“=”)
(填“>”“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农 业生产、生活中有着重要作用,
①如图是一定的温度和压强下N2和H2反应生成lmolNH3过程中能量变化示意图,请写出工业合成氨的热化学方程式:
(△H的数值用含字母Q1、Q2的代数式表示)
②氨气溶于水得到氨水,在25℃下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合,反应后溶液显中性,则c(NH4+)c(Cl-)(填“>”、“<”或“=”);用含a和b的代数式表示出该混合溶液中氨水的电离平衡常数.
(3)海水中含有大量的元素,常量元素如氯,微量元素如碘,其在海水中均以化合态存在,在25℃下,向0.1L0.002mol·L-l的NaCl溶液中逐滴加入适量的0.1L0.002mol·L-l硝酸银溶液,有白色沉淀生成,从沉淀溶解平衡的角度解释产生沉淀的原因是,向反应后的浊液中继续加入0.1L0.002mol·L-1的NaI溶液,看到的现象是,产生该现象的原因是(用离子方程式表示)。
(已知:25℃时KSP(AgCl)=1.6×l0-10KSP(AgI)=1.5×l0-16)
有关钴和铁化合物的性质见下表:
| 化学式 |
溶度积(室温时)Ksp |
沉淀完全时的pH |
氯化钴晶体的性质 |
| Co(OH) 2 |
5.9×10-15 |
9.4 |
CoCl2·6H2O呈红色,常温下稳定。110ºC~120ºC时脱水变成蓝色无水氯化钴 |
| Fe(OH) 2 |
1.6×10-14 |
9.6 |
|
| Fe(OH) 3 |
1.0×10-35 |
x |
用含钴废料(含少量铁)可制备氯化钴:Co+2HCl=CoCl2+H2↑工艺流程如下: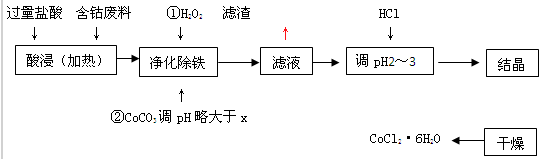
试回答:
(1)“净化除铁”中,写出加入CoCO3(难溶)调pH时反应的离子方程式
(2)滤液中(Fe3+)≤1.0×10-5mol/L时,可视为Fe3+沉淀完全。试计算室温下,Fe(OH) 3沉淀完全时,则x= 。
(3)②步中用CoCO3调pH略大于x的原因是 。
(4)滤液中所含溶质有 , 。
(5)为了防止CoCl2·6H2O脱水,“干燥”时宜采用的方法或操作是 , 。
已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出________kJ热量。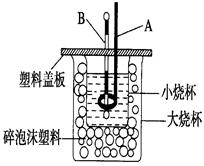
(2)如图装置中仪器A的名称是,碎泡沫塑料的作用是。
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ·mol-1,其原因可能是
。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会(填“偏大”、“偏小”、“无影响”)。