对于实验Ⅰ~Ⅳ的描述正确的是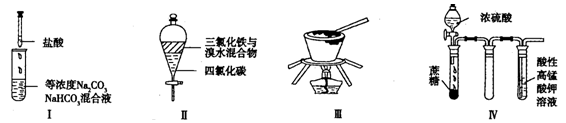
| A.实验Ⅰ:逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
| B.实验Ⅱ:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C.实验Ⅲ:从饱和食盐水中提取氯化钠晶体 |
| D.装置Ⅳ:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
一定温度下,可逆反应X(g)+3Y(g) 2Z(g)达到平衡的标志是
2Z(g)达到平衡的标志是
| A.正反应速率等于逆反应速率,且不等于零 |
| B.X的浓度不再发生变化 |
| C.Y的浓度不再发生变化 |
| D.Z的浓度不再发生变化 |
下列有关原子结构和元素周期律的表述正确的是
| A.原子序数为15的元素最高化合价为+5 |
| B.同周期元素中,VIIA族元素是非金属性最强的元素 |
| C.氧原子半径比氟原子半径大 |
| D.原子序数为12的元素位于元素周期表的第三周期IIA族 |
下列关于100mL 1mol·L-1 Na2CO3溶液的说法正确的是
| A.溶质N a2CO3质量为10.6g | B.用100mL 的容量瓶配制 |
| C.N a2CO3的摩尔质量为106g·mol-1 | D.量取水的体积小于100mL |
下列酸中,属于强酸的是
| A.硝酸 | B.盐酸 | C.硫酸 | D.高氯酸(分子式为HClO4) |
可用浓硫酸进行干燥的气体有
| A.SO2 | B.NH3 | C.HCl | D.CO2 |