用湿法制磷酸副产品氟硅酸(H2SiF6 )生产无水氟化氢的工艺如下图所示:
已知:氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于醇。在热水中水解成氟化钾、氟化氢及硅酸。
(1)写出反应器中的化学方程式:
(2)在实验室过滤操作中所用的玻璃仪器有: ;
在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是: ;
(3)该流程中哪些物质可以循环使用: (用化学式表达)
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6 ,试写出该反应方程式: ;
(5)为了测定无水氟化氢的纯度,取标况下的气体产物2.24L,测得质量为3.1g,并将气体通入含足量的Ca(OH)2 溶液中,得到5.85gCaF2沉淀,则无水氢氟酸质量分数为: 。(保留2位有效数字)通过计算结果,试解释,为什么标况下2.24L产物的质量远远大于2.0g, 。
某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。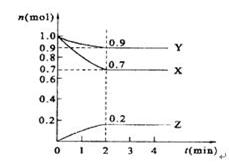
(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=,
(4)当反应进行到第min,该反应达到平衡。若三种物质都是气体,平衡时Y所占体积的百分比为______。
下表是稀硫酸与某金属反应的实验数据:
| 实验 序号 |
金属 质量/g |
金属 状态 |
c(H2SO4) /mol·L-1 |
V(H2SO4) /mL |
溶液温度/℃ |
金属消失的时间/S |
|
| 反应前 |
反应后 |
||||||
| 1 |
0.10 |
丝 |
0.5 |
50 |
20 |
34 |
500 |
| 2 |
0.10 |
粉末 |
0.5 |
50 |
20 |
35 |
50 |
| 3 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
250 |
| 4 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
| 5 |
0.10 |
粉末 |
0. 8 |
50 |
20 |
36 |
25 |
| 6 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
125 |
| 7 |
0.10 |
丝 |
1.0 |
50 |
35 |
50 |
50 |
| 8 |
0.10 |
丝 |
1.1 |
50 |
20 |
34 |
100 |
| 9 |
0.10 |
丝 |
1.1 |
50 |
20 |
44 |
40 |
分析上述数据,回答下列问题:
(1) 实验4和5表明_________对反应速率有影响;________,反应速率越快,能表明这一规律另一组实验是___________(填实验序号)。
(2) 在前4次实验中,能表明反应物浓度对反应速率产生影响的实验有________(填实验序号)。
(3) 本实验中影响反应速率的其他因素还有_________,其实验序号是_____。
(4) 实验中,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
_________________________________________________________。
有如下两个反应:
A 2HCl+Ba(OH)2===BaCl2+2H2O
B 2Fe3++Cu==2Fe2++Cu2+
(1) 根据两反应的本质,判断能否设计成原电池:AB(填“能”或“不能” )不能设计成原电池的原因是
(2) 根据能设计成原电池的反应选择适合的材料和试剂设计一个原电池
①负极材料是_______,正极材料是________,电解质溶液是 ___;
②写出负极的电极反应式 _;
③原电池工作时溶液中的Cl-从__________极向________极移动(填正或负)
④若导线上转移电子0.2mol,则负极质量变化是 ___ 减少 ___; 将此反应设计成原电池,若电解质溶液为H2SO4,
将此反应设计成原电池,若电解质溶液为H2SO4,
请写出正负极的电极反应;负极:_______________;正极:______________。
A、B、C、D、E、F六种元素为元素周期表中的前20号元素,0.5molA的元素的离子得到NA个电子后被还原为中性原子;0.4gA的氧化物恰好与100mL0.2mol/L的盐酸完全反应;A元素原子核内质子数与中子数相等。B元素原子核外电子数比A元素原子核外电子数多1;Cˉ离子核外电子层数比A元素的离子核外电子层数多1;D元素原子最外层电子数是次外层电子数的2倍;E的氯化物ECl21.11g配成溶液后,需用1mol/L的硝酸银溶液20mL才能把氯离子完全沉淀下来,且E的核内中子数为20;F的最高价氧化物对应的水化物可以与其氢化物发生反应生成盐。请填写下列空格:
(1)推断A、B、C、D、E、F六种元素的符号A_________;B_________;C________;D________; E_________;F_________
(2)C的一价阴离子的结构示意图__________________;
(3)D元素的最高价氧化物的结构式是_______________;
(4)C、D两元素形成的化合物电子式______________,分子内含有_______键(填极性或非极性)。
(5)55.5gECl2中所含质子的物质的量为__________mol。
下表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~ (4)小题用元素符号或化学式回答,(5)~(7)小题按题目要求回答。
| 族 周期 |
I A |
Ⅱ A |
Ⅲ A |
Ⅳ A |
Ⅴ A |
Ⅵ A |
Ⅶ A |
O |
| 1 |
A |
|||||||
| 2 |
D |
E |
G |
I |
||||
| 3 |
B |
C |
F |
H |
(1)表中元素,化学性质最不活泼的是,只有负价而无正价的是,氧化性最强的单质是,还原性最强的单质是.
(2)最高价氧化物的水化物碱性最强的是,酸性最强的是。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的,
(4)在B、C、E、F、G、H中,原子半径最大的是,
(5)A和E组成化合物类型(填“离子化合物”或“共价化合物”);它比A和F组成化合物的沸点(填“高”或“低”),原因是
(6)用电子式表示B的最高价氧化物对应的水化物的形成过程
(7)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式
。