(1)某学习小组收集到一些铜绿(碱式碳酸铜)他们拟通过化学反应获得铜,根据下图资料,回答下列问题。
①碱式碳酸铜的物理性质之一是 。
②用稀硫酸、铁为原料将碱式碳酸铜转化为铜,反应的化学方程式是: 。
(2)另一小组收集了一些硫酸铁与硫酸亚铁的混合物,如果经实验测知,硫酸铁与硫酸亚铁混合物中含硫a﹪,则其中含铁的质量分数为 。
(10株洲)23.(3分)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:(“O’’表示氧原子,‘‘●”表示氢原子,“ ’’表示氯原子)
’’表示氯原子)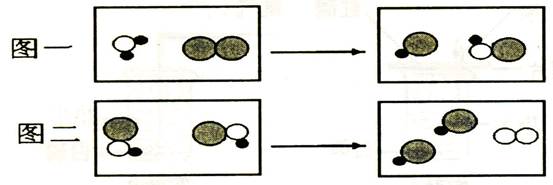
(1)上述图中所出现的物质中,共有种含有氧元素的化合物。
(2)从图中我们可知,在化学反应中,反应前后 个数不变。
(3)上述两个化学反应是否都属于四种基本反应类型:(填“是”或“否”)。
镁条在空气中燃烧,不仅生成氧化镁、氮化镁,还有少量镁与二氧化碳反应生成另一种单质和镁的氧化物。
(1)已知氮化镁中氮元素的化合价为-3价,请你写出氮化镁的化学式。
(2)写出镁与二氧化碳反应的化学方程式,
指出该反应的基本类型:反应。
(10连云港25)在上海世博园江苏馆的“春华秋实”展区,用我市东海水晶雕出的作品《寄畅园之冬》吸引了众多参观者的眼球。东海县石国家火炬计划硅胶材料产业化基地,产品由晶莹剔透的成分为SiO2)是制取高纯硅的主要原料,高纯硅又是制造计算机芯片的主要原料。
其生产过程示意图如下: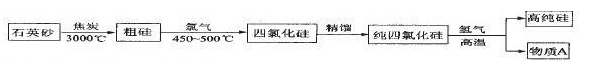
请你自学上述资料后,回答下列问题
(1)由石英砂制得高纯硅的反应原理中,属于化合反应的是填数字代号,下同),属于置换反应的是
(2)粗硅提纯必须在无氧的氛围中进行,除了考虑到硅易被氧化成二氧化硅外,还有一个原因是
(3)生产过程示意图中的“物质A”用水吸收,可得副产品(一种常见的酸)的名称是
(4)作为电器、电子、光纤等行业原料的石英砂纯度要求高,需要对普通石英砂(含有少量的CaCO3、Fe2O3)进行提纯,其中酸洗(用盐酸)和高纯水洗是两个最重要的步骤。请写出酸洗步骤中的一个反应的化学方程式(任写一个);判断高纯水洗是否洗净的方法是:取少量最后的洗涤液于试管中,向其中滴加AgNO3溶液,若无现象,则表明残留物已洗净;否则,表明残留物未洗净。
(3分)如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子。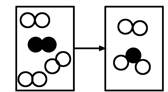
(1)反应后方框内应再填入1个微粒(选填序号)。
A.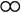 B.
B. C.
C.
(2)该反应所属的基本反应类型是反应。
(3)写出符合该微观示意图的一个具体反应的化学方程式
。