2012年4月15日,央视《每周质量报告》报道:一些企业用皮革废料熬制工业明胶,在加工过程中添加重铬酸钾,在加热条件下重铬酸钾分解,反应的化学方程式为:
4K2Cr2O7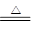 4K2CrO4+2X+3O2↑,工业明胶制造药用胶囊,导致胶囊重金属铬超标。铬是一种重金属元素,能对肝、肾等内脏器官和DNA造成损伤。在通常情况下,铬单质是银白色有金属光泽的固体,有较高的熔点,是最硬的金属;在加热时,能与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体。
4K2CrO4+2X+3O2↑,工业明胶制造药用胶囊,导致胶囊重金属铬超标。铬是一种重金属元素,能对肝、肾等内脏器官和DNA造成损伤。在通常情况下,铬单质是银白色有金属光泽的固体,有较高的熔点,是最硬的金属;在加热时,能与浓硫酸反应生成硫酸铬(其中铬元素化合价为+3价),同时还生成一种大气污染物和一种常见的液体。
回答下列问题:
(1)K2CrO4中铬元素的化合价是 ;K2Cr2O7分解生成X的化学式为 ;
(2)归纳铬单质的物理性质 ;
(3)铬单质与浓硫酸反应的化学方程式为 ;
(4)食品安全事件不断被报道,如:三聚氰胺、染色馒头等,在广大消费者中造成较大影响。面对事件要科学分析,正确判断。你认为下列认识缺乏科学性的是 (填字母序号)。
| A.使用了化学添加剂的食品对人体都有危害 |
| B.三聚氰胺、苏丹红、甲醛都是化工产品,食品安全事件都是化学惹得祸 |
| C.物质对人体的影响与摄入量有关,量变才能引起质变 |
| D.要合理膳食,使人体中各种常量、微量元素保持收支平衡 |
根据下列实验装置图填空:
(1)图中标有序号仪器的名称:①,②。
(2)实验室用石灰石和稀盐酸制取二氧化碳时,反应的化学方程式为:,应选用的发生装置是(填装置序号,下同)。
(3)甲烷是一种无色无味、难溶于水、密度比空气小的气体.实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷时,发生装置应选用,收集装置应选用。
在原子、分子水平上研究物质及其变化是学习化学的基础.下列图示为部分化学反应的微观示意图。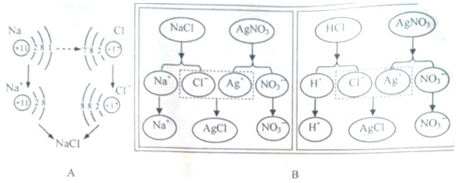
请据图回答:
(1)图
是金属钠与氯气反应生成氯化钠的微观示意图.由图可以看出:元素的化学性质与原子的关系密切;氯化钠是由构成的.工业上可用氯化钠生产一种常用的碱,即氯化钠饱和水溶液在通电的条件下反应,生成这种碱、氯气(
)和氢气,该反应的化学方程式为。
(2)图
示氯化钠溶液和稀盐酸分别于硝酸银溶液反应的微观示意图.由图可知,这两个反应在微观实质上的共同点是。
某化工厂的废液中含有硝酸银、硝酸亚铁和硝酸锌.某同学取适量的上述废液样品,将一定质量的镁粉加入样品中,充分反应后过滤,得到滤液和滤渣.请填空:
(1)若得到的滤液为浅绿色,则滤液中的溶质一定含有(填写化学式,下同),可能含有。
(2)若得到的滤液为无色,则滤渣中至少含有种金属。
(3)反应后得到滤渣的质量(选填"小于"、"大于"或"等于")反应前加入镁粉的质量。
材料的应用,极大地促进了人类社会的发展和人们生活水平的提高.请从化学视角回答下列问题:
(1)如图是某品牌服装标签的部分内容.请根据标签提供的信息回答:
在面料中,属于有机合成纤维的是.区分羊毛与涤纶的简单实验方法是(选填"观察光泽"或"灼烧闻气味"。
(2)请列举合成橡胶在生产生活中的一种具体用途:。
(3)塑料常用于制作食品保鲜膜及方便袋等,极大的方便了我们的生活,但大量使用后随意丢弃会造成"白色污染"。为了保护环境,减少"白色污染",请结合日常生活提出一条合理化建立:。
化学物质及其变化与人类生产、生活密切相关,请填写下列空格:
(1)现有水、氮气、氧气、铁四中物质,其中:(填写化学式)
①可供给人类呼吸的是。②可作溶剂,对生命活动具有重要作用的是。
③可用于食品防腐的是。④应用最广泛的金属是。
(2)用化学方程式表示:
①水在通电作用下的反应:。②细铁丝在氧气中燃烧的反应:。