甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g);ΔH=+49.0 kJ/mol
②CH3OH(g)+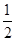 O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ/mol
O2(g)===CO2(g)+2H2(g);ΔH=-192.9 kJ/mol
下列说法正确的是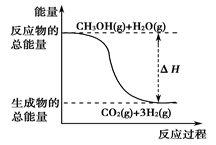
| A.CH3OH的燃烧热为192.9 kJ/mol |
| B.反应①中的能量变化如上图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
D.根据②推知反应CH3OH(l)+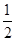 O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol |
下列关于物质的量、摩尔质量的叙述正确的是 ( )
| A.0.012 kg12C中含有约6.02×1023个碳原子 |
| B.1 mol H2O中含有2 mol氢和1 mol氧 |
| C.氢氧化钠的摩尔质量是40 g |
| D.2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |
下列说法正确的是 ( )
| A.摩尔就是物质的量 |
| B.物质的量的单位是kg·mol-1 |
| C.HNO3的摩尔质量是63 g |
| D.1 mol H2O的质量为18 g |
某化学兴趣小组欲研究H2SO4、NaCl、KCl、Na2CO3、NaOH的性质,对于如何研究,他们设计了两种研究方案:
方案①:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验;
方案②:将它们按照钠盐、钾盐和其他化合物分类,然后分别溶于水得到溶液,进行实验。下列说法正确的是 ( )
| A.常温时将少量铜粉分别投入上述溶液中,按照方案①的分类,能够完全溶解铜粉的只有稀硫酸溶液 |
| B.设计方案②的同学取某种溶液,在其中加入上述的钾盐溶液,有白色沉淀生成,再加入稀硝酸,沉淀不消失,则该溶液中含有Ag+ |
| C.按照方案①的分类,属于碱的有Na2CO3、NaOH |
| D.这两组同学在研究物质时不仅仅使用了实验法、观察法 |
下列关于酸性氧化物、碱性氧化物、单质、混合物的分类中,正确的是 ( )
| 酸性氧化物 |
碱性氧化物 |
单质 |
混合物 |
|
| A |
干冰 |
Na2O |
金刚石 |
浓盐酸 |
| B |
CO |
Fe3O4 |
溴 |
漂白粉 |
| C |
SO2 |
Na2O2 |
石墨 |
福尔马林 |
| D |
SO3 |
Fe2O3 |
硫黄 |
FeSO4·7H2O |
以下表示的是碳及其化合物的相互转化关系:
C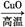 CO2
CO2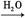 H2CO3
H2CO3 CaCO3
CaCO3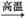 CO2
CO2
其中涉及的基本反应类型依次为 ( )
| A.置换、化合、分解、复分解 |
| B.置换、化合、复分解、分解 |
| C.化合、置换、分解、复分解 |
| D.化合、置换、复分解、分解 |