短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.元素X 的简单气态氢化物的热稳定性比W的弱 |
| B.元素W 的最高价氧化物对应水化物的酸性比Z的弱 |
| C.原子半径的大小顺序: rY >rZ >rW >rX |
| D.化合物YX、ZX2、WX3中化学键的类型相同 |
有关下图所示化合物的说法不正确的是( )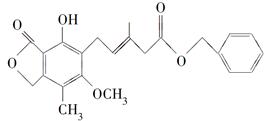
| A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 |
| B.1 mol该化合物最多可以与3 mol NaOH反应 |
| C.既可以催化加氢,又可以使酸性KMnO4溶液褪色 |
| D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
下列说法正确的是( )
A.已知:H2(g)+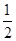 O2(g)===H2O(l);ΔH=-285.8 kJ·mol-1 ,则H2的燃烧热为-285.8 kJ·mol-1 O2(g)===H2O(l);ΔH=-285.8 kJ·mol-1 ,则H2的燃烧热为-285.8 kJ·mol-1 |
| B.已知:S(g)+O2(g)===SO2(g) ΔH1=-Q1 ;S(s)+O2(g)===SO2(g) ΔH2=-Q2,则Q1<Q2 |
C.已知: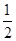 H2SO4(浓)+NaOH(aq)="==" H2SO4(浓)+NaOH(aq)="==" 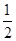 Na2SO4(aq)+H2O(l) ΔH1; Na2SO4(aq)+H2O(l) ΔH1;CH3COOH(aq)+NH3·H2O(aq)===CH3COONH4(aq)+H2O(l) ΔH2,则有|ΔH1|<|ΔH2| |
| D.已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g)ΔH=+489.0 kJ·mol-1 |
CO(g)+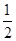 O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)===CO2(g) ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)===2Fe2O3(s) ΔH=-1641.0 kJ·mol-1
下列离子方程式与所述事实相符且正确的是()
| A.磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-=3Fe3++NO↑+4H2O |
| B.Ca(HCO3)2溶液中加入少量NaOH溶液: Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| C.明矾溶液中加入Ba(OH)2溶液至生成的沉淀物质的量最多: Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| D.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应: |
4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3-(aq), 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是()
I3-(aq), 某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是()
A.反应 I2(aq)+I-(aq) I3-(aq)的 △H>0 I3-(aq)的 △H>0 |
| B.若温度为T1、T2时,反应平衡常数分别为K1、K2,则K2>K1 |
| C.若反应进行到状态D时,一定有v正>v逆 |
| D.状态A与状态B相比,状态A的c(I2)大 |
下列实验操作中一定会造成实验值偏小的是( )
| A.将pH试纸用蒸馏水湿润后测某溶液的pH |
| B.配制500mL 0.10mol/L NaCl溶液,定容时俯视 |
| C.以标准盐酸溶液滴定未知浓度的NaOH溶液时,酸式滴定管未用标准溶液润洗 |
| D.用标准NaOH溶液滴定未知浓度的盐酸溶液,开始时滴定管尖嘴处没有气泡,结束时有气泡 |