电子工业常用30%的FeCl3溶液腐蚀覆盖有一薄层铜的绝缘板,制成印刷电路板。人们为了从废腐蚀液(含有CuCl2、FeCl2和FeCl3)中回收铜,并重新得到FeCl3溶液,设计如下实验流程。
已知:2FeCl3 + Fe = 3FeCl2
(1)操作②、④的名称是_______。
(2)上述流程中,X的化学式为 __ ,滤渣中所含的物质是_______,步骤③中有关反应的化学方程式为_______。
(3)Z为氯气,第⑥步发生的反应为化合反应,此反应的化学方程式为 。
鸡蛋壳的主要成分是碳酸钙(其它成分不溶于水也不与酸反应)。化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,做如下实验:
反应①结束后,所加盐酸刚好反应了一半,反应②恰好完全反应。请回答下列问题:
(1)反应①的化学方程式为;
(2)根据已知条件列出求解碳酸钙质量(
)的比例式;
(3)该鸡蛋壳中碳酸钙的质量分数为;
(4)所加氢氧化钙的质量为;
(5)溶液
中溶质的质量分数为;
(6)用36.5%的浓盐酸配制
上述稀盐酸需加水的质量为。
下图中的六个圆
、
、
、
、
、
分别表示六种物质,蓝色溶液
与
反应能生成两种沉淀,
为氧化物,
、
、
、
分别是碳酸钠溶液、稀硫酸、氢氧化钡溶液和氢氧化钠溶液中的一种,
中溶质可用于生产洗涤剂。用"→"表示一种物质能转化为另一种物质,用两圆相切或"--"表示两种物质可以发生化学反应,六种物质之间的部分反应及转化关系如右图所示。请利用初中化学知识回答下列问题: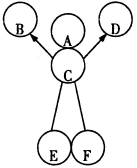
(1)在图中标出六种物质(或溶质)的化学式;
(2)
与
反应的化学方程式为;
(3)
与
反应的实验现象为。
硬水受热后会产生水垢,水垢的主要成分是
和
,其它成分不参与反应。实验室由水垢制取纯净
固体的流程如下: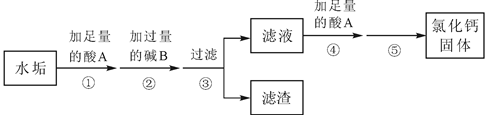
请按要求填空:
(1)酸
是人体胃酸的主要成分,酸
的化学式是;
(2)步骤②中生成沉淀的化学反应方程式是;
(3)步骤④加酸
的作用是;
(4)步骤⑤是利用的方法得到氯化钙固体。
是初中化学常见物质。其中,
的浓溶液能挥发出刺激性气味的气体,从
的反应过程中有蓝色沉淀生成,
为白色沉淀。下图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。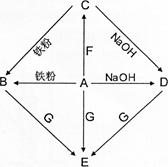
(1)请写出化学式:
,
。
(2)写出
的化学方程式:。
(3)在
的反应过程中,
与
溶液恰好完全反应,反应后所得溶液的
7(填">"、"="或"<")。
(4)
溶液与铁粉反应后,取剩余固体加入盐酸,没有气体放出。请分析:
与铁粉反应后的溶液组成中除了
外,一定存在的物质有,可能存在的物质有。
(7分)过氧化钙(CaO2)难溶于水,常温下稳定,在潮湿空气及水中缓慢放出氧气,广泛应用于渔业等领域。下图是以大理石(含Al2O3及其他不溶于水也不溶于酸的杂质)等为原料制取CaO2的流程图: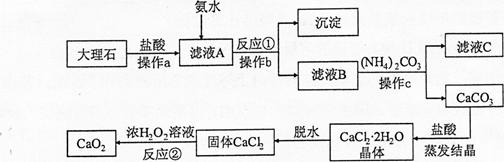
(1)操作a、b、c的名称都是 。
(2)操作a的目的是 。
(3)从滤液C中可回收的副产品的化学式为 。
(4)写出反应①的化学方程式 。
(5)反应②的基本反应类型是 。
(6)在该生产过程中,用110kg大理石制得了72Kg的过氧化钙。如果不考虑过程中的损耗,可计算出大理石中CaCO3的质量分数为 。(结果保留一位小数)