某学校实验室的废液缸中收集了学生在实验室制取二氧化碳后残留的废液。小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么物质?
【做出猜想】(1)小红认为废液中的溶质只有CaCl2。你认为还可能含有的物质是 。(填化学式)。
【查阅资料】CaCl2溶液呈中性。
【实验与结论】(1)小红取少量残留废液和少量氯化钙溶液分别加入到两支试管中,并分别滴入无色酚酞试液做对比实验,结果两支试管中溶液均无色,于是小红认为自己的猜想是正确的。
(2)你认为小红的实验 (填“能”或“不能”)证明他的猜想是正确的,理由是 。
(3)如果要证明你的猜想是正确的,你选择的试剂是 (与小红所用试剂类别不同),当加入该试剂时观察到的现象是 。
【拓展应用】若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的 ,反应完全后过滤。
(4)通过以上探究你认为实验室的废液未经处理直接导入下水道,可能造成的危害是 (写一条)。
某兴趣小组利用氨水能使酚酞试液变红的原理,设计如下实验以探究微粒的运动。请回答实验中的有关问题。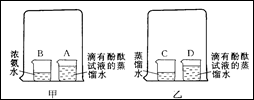
(1)实验I:在盛有少量蒸馏水的小烧杯中滴入2滴~3滴酚酞试液,再向其中滴加浓氨水。由实验I得出的结论有
(2)实验Ⅱ(如上图中甲所示):烧杯A中的现象是;产生这一现象的原因是。
(3)为使实验结论准确可靠,该兴趣小组设计实验Ⅲ(如上图中乙所示)作为对比实验。你认为有无必要,理由是。
同学们已经学习了有关金属的一些知识,对金属的活动性顺序也有 了一定的认识。请运用所学知识参与以下探究并回答相关问题:
【 实验一】将4枚洁净无锈的铁钉分别放入图12中 a、b、c、d 4支试管中。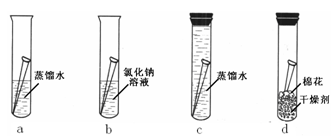
上述实验中,____________试管中的铁钉最易生锈。设计如图d实验的目的是________
________________________________________。铁生锈的主要原因是铁与、
等物质发生了复杂的化学反应。
【 实验二】为了探究Fe、Cu、Al三种金属的活动性顺序,小宁同学做了图13所示的实验.
(1)实验时,为了除去铝和铁表面的氧化物或污物,在插入溶液前应将。
(2)实验时观察到的主要现象是。得出的结论是______________________________。写出其中一种金属与硫酸铜溶液反应的化学方程式。
(3)小成同学认为小宁同学设计的实验不能达到实验目的,原因是
,因此另设计一个实验,才能得出正确的结论。请你设计一个实验并完成下表:
| 操作 |
现象 |
结论 |
| 三种金属活动性由强到弱的顺序是:Al 、Fe、Cu |
某化学兴趣小组按照课本实验方法(如下图),做木炭与氧化铜反应的实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。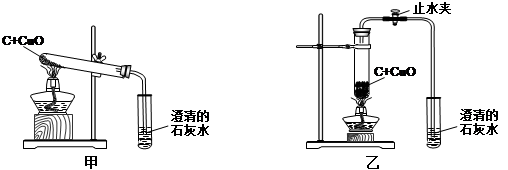
【提出问题】暗红色的固体是什么?如何选择合适条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
【猜想与假设】
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
【分析与交流】
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是;
反应的化学方程式为:。
(2)小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是
。
【实验与结论】
同学们决定按改进后的方案进行实验,他们在检验了乙装置的后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是(填“吸”或“放”)热反应。
待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①II中x的值为 .
②若要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的 和 都不改变.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2的体积 |
| I |
50.0g |
1% |
0.1g |
9mL |
| II |
50.0g |
2% |
0.1g |
16mL |
| III |
50.0g |
4% |
0.1g |
31mL |
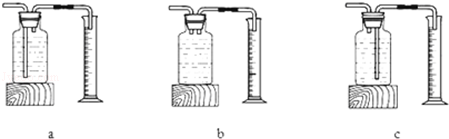
①若用上述装置测生成氧气的体积,则用图 (填“a”“b”或“c”)
②实验结论:在相同条件下, ,双氧水分解得快.
在化学实验室里,酒精是最常用到的一种燃料,其化学式是C2H6O。小明为了证明酒精中含有碳、氢元素,设计并完成如下实验方案。请你帮他完成下面的实验报告。
【实验目的】:证明酒精中含有碳、氢元素。
【实验用品】:酒精灯、火柴、洁净干燥的小烧杯、澄清石灰水
【实验过程及结论】
| 实验步骤 |
实验现象 |
实验结论 |
步骤一:点燃酒精灯,将洁净干燥的小烧杯罩在火焰上方 |
烧杯内壁 有生成; |
证明酒精中含有元素 |
步骤二:迅速取下烧杯,并加入少量,振荡; |
证明酒精中含有碳元素 |