E~N等元素在周期表中的相对位置如下表。E与K的原子序数相差5,K是地壳中含量最多的元素,下列判断不正确的是
| E |
|
|
|
K |
| F |
G |
|
M |
L |
| |
H |
|
N |
|
A.E与K化合可以生成两种化合物
B.氢化物的稳定性和沸点:K>L>M
C.H与N的原子核外电子数相差3
D.最高价氧化物的水化物碱性:F>G
下列反应的离子方程式不正确的是
| A.向NaClO溶液中通入少量SO2气体:3ClO-+SO2+H2O═SO42-+Cl-+2HCl |
| B.将过量的Cl2通入FeBr2溶液中:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
| C.向碳酸氢钙溶液中滴加氢氧化钠溶液至Ca2+恰好完全:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D.向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液至沉淀量最大: |
NH4++Al3++2SO42-+4OH-=Al(OH)3↓+2BaSO4↓+NH3·H2O
下列实验方案可行的是
| A.检验NH4+时,加浓NaOH溶液,加热,用湿润的红色石蕊试纸放在试管口检验,若试纸变蓝,则可证明原溶液中含有NH4+ |
| B.检验SO42-时,加入BaCl2溶液,再加稀硝酸,若沉淀不消失,则可证明含SO42- |
| C.用天平和小烧杯称量5.40gNaOH固体 |
| D.用饱和FeCl3溶液中逐滴滴加NaOH溶液,至溶液呈红褐色即可制得Fe(OH)3胶体 |
下列推论正确的是
| A.S(g)+O2(g)=SO2(g) △H1,S(s)+O2(g)=SO2(g)△H2;△H1>△H2 |
| B.C(石墨,s)=C(金刚石,s) △H=+1.9kJ/mol,则可判定金刚石比石墨稳定 |
| C.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测出的中和热数值偏小 |
| D.已知反应:①101kPa时,2C(s)+O2(g)="2CO(g)" △H=-221kJ/mol,则C的燃烧热为110.5kJ/mol |
下列有关实验的选项正确的是
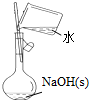
| A.配制0.10mol•L-1NaOH溶液 |
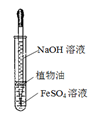
B.制备Fe(OH)2沉淀 |
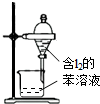
C.苯萃取碘水中的I2,分出水层后的操作 |
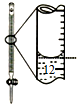
D.记录滴定终点读数为12.20mL |
 |
 |
 |
 |
下列关于物质分类的组合正确的是
| 分类 |
纯净物 |
混合物 |
强电解质 |
弱电解质 |
非电解质 |
| A |
重水 |
氨水 |
氯化钾 |
碳酸钙 |
二氧化碳 |
| B |
冰醋酸 |
漂白粉 |
硫酸钡 |
氟化氢 |
氨气 |
| C |
胆矾 |
水泥 |
苛性钠 |
亚硫酸 |
石灰石 |
| D |
氯化氢 |
分馏汽油 |
硝酸 |
醋酸 |
氯气 |