常温下,盐酸和一元碱MOH溶液等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 |
起始浓度/(mol·L-1) |
反应后溶液的pH |
|
| c(HCl) |
c(MOH) |
||
| ① |
0.1 |
0.1 |
5 |
| ② |
0.2 |
x |
7 |
| ③ |
0.1 |
0.2 |
10 |
| ④ |
0.2 |
0.1 |
y |
下列判断正确的是
A.实验①反应后的溶液中:c(MOH)约为1×10—5mol·L-1
B.实验②反应后的溶液中:c(MOH)>c(M+)=c(Cl-)>c(H+)=c(OH-)
C.实验③反应后的溶液中:c(M+)+c(H+)=c(OH-)+c(MOH)
D.实验④反应后的溶液中:c(H+)-c(OH-)-c(MOH)=0.05 mol·L-1
有机物M的结构简式为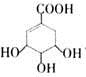 ,下列说法不正确的是
,下列说法不正确的是
| A.M的分子式为:C7H10O5 | B.M与乙酸互为同系物 |
| C.M可使溴的四氯化碳溶液褪色 | D.M在一定条件下可发生取代反应 |
设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.4.0 g重水(D2O)中所含中子数为1.6 NA |
| B.1 L 2 mol·L-1 K2S溶液中S2-和HS-的总数为2 NA |
| C.2.4g金刚石与石墨的混合物中所含碳原子数为0.2 NA |
| D.50 mL 18 mol·L-1浓硫酸与足量铜反应,转移的电子数为0.9 NA |
下列有关说法正确的是
| A.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
C.反应N2(g)+3H2(g) 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大 2NH3(g)△H<0平衡时,其他条件不变,升高温度,再次达到平衡时氢气转化率增大 |
D.吸热反应“TiO2(s)+2Cl2(g) TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反应的△S<0 |
右图为元素周期表短周期的一部分,E原子的电子层数为n,最外层电子数为2n+1下列述不正确的是
| A |
B |
C |
|
| D |
E |
A.C和E氢化物的热稳定性和还原性均依次减弱
B.A与B形成的阴离子可能有AB32- A2B42-
C.AD2分子中每个原子的最外层均为8电子结构
D.A、D、E的最高价氧化物对应的水化物的酸性依次增强
、 的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)
的同分异构体中,某苯环上的一氯代物只有一种的结构有(不考虑立体异构)
| A.6种 | B.5种 | C.4种 | D.3种 |