下列离子方程式书写不正确的是
| A.向溴化亚铁溶液中通入过量氯气:2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl- |
| B.NaHCO3溶液中滴加少量澄清石灰水:2HCO3-+Ca2++2OH-= CaCO3↓+2H2O+ CO32- |
| C.过量铁粉与稀HNO3反应:3Fe+8H++2NO3-= 3Fe2++2NO↑+4H2O |
| D.0.01 mol/LNH4Al(SO4)2溶液与0.02 mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
下列表述中正确的是
| A.任何能使熵值增大的过程都能自发进行 |
| B.△H<0,△S>0的化学反应一定能自发进行 |
C.已知热化学方程式2SO2(g)+O2(g) 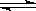 2SO3(g)△H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量 2SO3(g)△H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量 |
| D.稀溶液中1mol NaOH分别和1mol CH3COOH、1molHNO3反应,两者放出的热量一样多 |
下列有关化学实验操作正确的是_(填序号)
①实验室进行石油的分馏实验时,温度计水银球插入石油液面以下
②由于碘在乙醇中的溶解度较大,用乙醇萃取分离溶于水中的碘。
③验证RX是碘代烷,把RX与烧碱水溶液混合加热后,将溶液冷却后再加入硝酸银溶液。
④实验室用无水乙醇和浓硫酸共热制乙烯时,把温度计水银球插入液面以下。
⑤分离苯和苯酚的混合液,先加入适量浓溴水,再过滤、分液,即可实现。
某有机化合物A的相对分子质量大于100,小于130。经分析得知,其中碳和氢的质量分数之和为46.66%,其余为氧,则该化合物分子中最多含碳氧双键的个数为
| A.1 | B.2 | C.3 | D.4 |
甲醛、乙酸和丙醛组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为
| A.27% | B.28% | C.54% | D.无法计算 |
阿魏酸在食品、医药等方面有若干广泛用途。一种合成阿魏酸的反应可表示为
下列说法正确的是
| A.可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 |
| B.香兰素、阿魏酸均可与Na2CO3、NaOH、NaHCO3溶液反应 |
| C.香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D.与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |