用NA表示阿伏加德罗常数,下列说法正确的是
| A.在标准状况下,44.8L HF所含有的分子数为2NA |
| B.含2mol H2SO4的浓硫酸与足量铜微热反应,生成SO2分子数为NA |
| C.常温常压下,44g由N2O和CO2组成的混合气体所含的分子数为NA |
| D.1mol羟基和1molOH-含有的电子数都为10NA |
Mg—AgCl电池是一种用海水激活的一次电池,在军事上用作电动鱼雷的电源.电池的总反应可表示为:Mg+2AgCl═MgCl2+2Ag下列关于该电池的说法错误的是
| A.该电池工作时,正极反应为:2AgCl+2e-═2C1-+2Ag |
| B.该电池的负极材料可以用金属铝代替 |
| C.有24g Mg被氧化时,可还原得到108gAg |
| D.装备该电池的鱼雷在水中行进时,海水作为电解质溶液 |
下列表示对应化学反应的离子方程式正确的是
| A.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O===3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-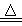 NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中:SO2+NH3·H2O===HSO3-+NH4+ |
| D.足量草酸与KOH反应:H2C2O4+2OH- === C2O42-+2H2O |
短周期主族元素A、B、C、D原子序数依次增大,已知A、C同主族,且A、B、C三种元素最外层电子数之和为15,B原子最外层电子数为A原子最外层电子数的一半,下列叙述正确的是
A.原子半径A<B<C<D
B.2.32gFe3O4与足量B单质完全反应,转移0.09mol电子
C.常温下,B、D形成的化合物的水溶液pH<7
D.简单气态氢化物稳定性C>D
始祖鸟烯形状宛如一只展翅飞翔的鸟,其键线式结构表示如图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是
| A.始祖鸟烯与CH2===CH-CH===CH2互为同系物 |
| B.若R1=R2=甲基,则其化学式为C12H16 |
| C.若R1=R2=甲基,在一定条件下烯烃双键上的碳原子上的氢也能取代,则始祖鸟烯的一氯代物有3种 |
| D.始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,且两反应的反应类型是相同的 |
下列实验不能达到预期目的的是

| A.利用Ⅰ装置检查气密性,打开分液漏斗活塞,液体顺利流下 |
| B.利用Ⅱ装置制取NH3 |
| C.利用Ⅲ装置进行铜与浓硝酸反应的实验 |
| D.利用Ⅳ装置收集NH3 |