【改编】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,2.24 L NH3分子中共价键数目为0.3 NA |
| B.1molFe与足量的氯气反应,转移的电子数目为2NA |
| C.标准状况下,2.24LSO3的质量约为8g |
| D.1 L 0.1 mol·L-1NH4Cl溶液中NH4+数目为0.1 NA |
β—月桂烯的结构如右图所示,一分子该物质与两分子溴发生加成反应的产物(只考虑位置异构)理论上最多有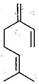
| A.2种 | B.3种 | C.4种 | D.6种 |
下列实验装置图及实验用品均正确的是(部分夹持仪器未画出)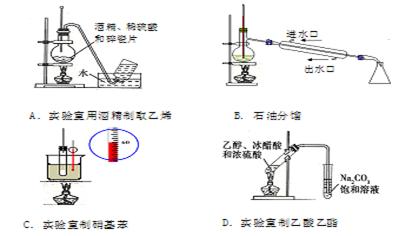
下列叙述正确的是
| A.乙醇、丙三醇互为同系物,同系物之间不可能互为同分异构体 |
| B.蛋白质的变性和盐析都是不可逆的过程 |
| C.乙酸乙酯、油脂与NaOH溶液反应均有醇生成 |
| D.淀粉、油脂、纤维素、蛋白质都能水解,但水解产物都不同 |
下列离子方程式正确的是
| A.往硝酸银溶液中滴加少量氨水:Ag++2NH3==[Ag(NH3)2]+ |
B.尼泊金酸(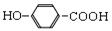 )与碳酸氢钠溶液反应: )与碳酸氢钠溶液反应: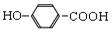 +2HCO3— → +2HCO3— →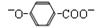 + 2CO2↑+2H2O + 2CO2↑+2H2O |
C.乙醛的银镜反应:CH3CHO+2[Ag(NH3)2]++2OH- CH3COO-+NH4++2Ag↓+3NH3+H2O CH3COO-+NH4++2Ag↓+3NH3+H2O |
| D.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
下列叙述正确的是
A. Fe分别与氯气和稀盐酸反应所得氯化物相同
B. K、Zn分别与少量的稀硫酸反应所得溶液均呈中性
C. Li、Na、K的原子半价和密度随原子序数的增加而增大
D. C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强