【原创】25℃时,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Na+、K+、MnO4-、I- |
| B.与铝反应生成氢气的溶液中:Na+、NH4+、AlO、Cl— |
| C.0.1mol/LNa2SO3溶液中:K+、NO3-、S2-、Cl— |
| D.中性溶液中:Cu2+、Na+、Br‾、SO42‾ |
一定条件下,在容积为10L的密闭容器中,将1mol X和1tool Y进行如下反应:2X(g)+Y(g)  Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
Z(g),经60s达到平衡生成0.3mol的Z,下列说法正确的是( )
| A.60 s时Z的平衡浓度为O.03mol/L |
| B.将容器容积变为20 L,Z的新平衡浓度将等于原平衡浓度的一半 |
| C.若温度和体积不变,往容器内增加1 mol Y,Y的转化率将增大 |
| D.若升高温度,X的体积分数增大,则正反应的△H>O |
已知热化学方程式:SO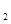 (g)+
(g)+ 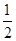 O
O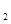 (g)
(g)  SO
SO (g)△H=-98.32kJ·mol
(g)△H=-98.32kJ·mol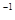 ,在容器中充人2molSO
,在容器中充人2molSO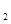 和1molO
和1molO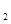 充分反应,最终放出的热量为 ( )
充分反应,最终放出的热量为 ( )
| A.196.64kJ | B.196.64 kJ·mol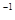 |
C.<196.64kJ | D.>196.64kJ |
在0.1mol/L的醋酸溶液中存在如下电离平衡:CH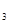 COOH
COOH CH
CH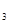 COO
COO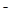 +H
+H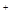 ,对于该平衡,下列说法正确的是 ( )
,对于该平衡,下列说法正确的是 ( )
A.该溶液pH增大时,CH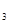 COO COO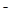 浓度可能增大也可能减小 浓度可能增大也可能减小 |
| B.滴加少量的O.1mol/L的盐酸溶液,溶液中氢离子浓度减小 |
| C.加入少量的醋酸钠固体,平衡向正反应方向移动 |
D.加入水稀释c(CH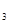 COO COO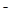 )·c(H )·c(H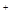 )/c(CH )/c(CH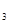 COOH)变大 COOH)变大 |
下列说法与盐的水解有关的是 ( )
①明矾可以傲净水剂;
②实验室配制FeCl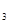 溶液时,往往在FeCl
溶液时,往往在FeCl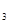 溶液中加人少量的盐酸;
溶液中加人少量的盐酸;
③用NaHCO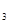 和A1
和A1 (SO
(SO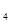 )
)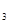 两种溶液可作泡沫灭火剂;
两种溶液可作泡沫灭火剂;
④在NH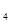 Cl溶液中加入金属镁会产生氢气;
Cl溶液中加入金属镁会产生氢气;
⑤草木灰与氨态氮肥不能混合施用;
⑥实验室盛放Na CO
CO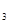 溶液的试剂瓶应用橡皮塞;
溶液的试剂瓶应用橡皮塞;
⑦纯碱溶液去油污;
| A.①③⑥ | B.②③⑤ | C.③④⑤ | D.全部有关 |
下列各离子方程式属于水解反应,且可使溶液呈酸性的是 ( )
A.HS +H +H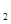 0 0 H H O O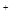 +s +s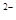 |
B.NH +2H +2H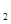 O O NH3·H NH3·H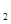 O+H O+H O+ O+ |
C.HCO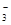 +OH +OH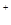  CO CO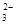 +H +H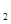 O O |
D.CO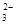 +2H +2H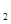 O O H H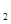 CO CO +2OH +2OH |