【改编】下列实验中,依据实验操作及现象得出的结论正确的是
| |
操 作 |
现 象 |
结 论 |
| A |
用pH试纸测定等浓度的Na2CO3和NaClO溶液的pH |
后者pH比前者的大 |
酸性:碳酸>次氯酸 |
| B |
常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸 |
有少量气泡产生 |
常温下Ksp(BaCO3)<Ksp(BaSO4) |
| C |
向溶液X中加入稀硝酸,并将产生的无色气体通入澄清石灰水中 |
生成白色沉淀 |
溶液X中一定含有CO32—或HCO3— |
| D |
向醋酸钠溶液中滴入酚酞试液,加热 |
溶液红色加深 |
醋酸钠水解是吸热的 |
M 2+离子有2个电子层,则M在周期表的位置是()
| A.第二周期零族 | B.第二周期Ⅷ族 | C.第二周期ⅡA族 | D.第三周期ⅡA族 |
2007年诺贝尔化学奖得主Gerhard Ertl对金属Pt表面催化CO氧化反应的模型进行了深入研究。下列关于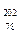 Pt的说法正确的是()
Pt的说法正确的是()
A.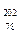 Pt和 Pt和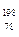 Pt的质子数相同,互称为同位素 Pt的质子数相同,互称为同位素 |
B.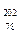 Pt和 Pt和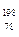 Pt的中子数相同,互称为同位素 Pt的中子数相同,互称为同位素 |
C.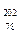 Pt和 Pt和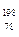 Pt的核外电子数相同,是同一种核素 Pt的核外电子数相同,是同一种核素 |
D.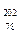 Pt和 Pt和 Pt的质量数不同,不能互称为同位素 Pt的质量数不同,不能互称为同位素 |
化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是 ( )
| A.为提高农作物的产量和质量,应大量使用化肥和农药 |
| B.绿色化学的核心是应用化学原理对环境污染进行治理 |
| C.实现化石燃料清洁利用,就无需开发新能源 |
| D.垃圾是放错地方的资源,应分类回收利用 |
常见镍氢电池的某极是储氢合金LaNi5H6(LaNi5H6中各元素化合价均为零),电池反应通常表示为:LaNi5H6+6NiO(OH)  LaNi5+6Ni(OH)2,下列说法不正确的
LaNi5+6Ni(OH)2,下列说法不正确的
| A.放电时储氢合金作正极 |
| B.放电时负极反应:LaNi5H6 + 6OH-- 6e-= LaNi5 + 6H2O |
| C.充电时阳极周围c(OH-)增大 |
| D.充电时储氢合金作阴极 |
下列各溶液中,微粒的物质的量浓度关系正确的是
| A.0.1mol·L-1的(NH4)2SO4溶液中:c(SO42- )>c(NH4+ )>c(H+)>c(OH-) |
| B.0.2mol·L-1的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C.0.1mol·L-1的NH4Cl溶液与0.05mol· L-l的NaOH溶液等体积混合: c(Cl- ) >c(Na+ ) >c(NH4+ ) >c(OH- ) >c(H+) |
| D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4C1溶液: |
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4C1)