甲、乙组同学分别做了以下探究实验。
(1)甲组探究Cl2与Na2SO3溶液反应,实验装置如下。

①请指出该装置的不足之处 、 。
②Cl2与Na2SO3溶液反应的离子方程式为 。
③设计实验,简述实验步骤,证明洗气瓶中的Na2SO3已被氧化 。
乙组探究乙酸乙酯(沸点77.1℃)在不同温度、不同浓度NaOH溶液中的水解速率。
取四支大小相同的试管,在试管外壁贴上体积刻度纸,按下表进行对照实验。在两种不同温度的水浴中加热相同时间后,记录酯层的体积来确定水解反应的速率。
| 实验 试剂 |
试管Ⅰ(55℃) |
试管Ⅱ(55℃) |
试管Ⅲ(55℃) |
试管Ⅳ(75℃) |
| 乙酸乙酯/mL |
1 |
V1 |
V2 |
V2 |
| 1mol·L—1NaOH/mL |
V4 |
3 |
0 |
V5 |
| 蒸馏水/mL |
0 |
V6 |
5 |
2 |
④请完成上表,其中V2 = ,V4= ,V5= 。
⑤实验中,可用饱和食盐水替代蒸馏水,其优点是 ;但不能用饱和Na2CO3溶液替代蒸馏水,其原因是 。
⑥实验中,试管Ⅳ比试管Ⅱ中的酯层减少更快,其原因有:温度高速率快,还可能有 。
甲、乙两同学欲分别完成“钠与氯气反应”的实验。
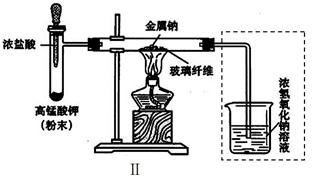

Ⅰ.甲同学的方案为:取一块绿豆大的金属钠(除去氧化层),用滤纸吸净煤油,放在Ⅰ石棉网上,用酒精灯微热。待钠熔成球状时,将盛有氯气的集气瓶抽去玻璃片后倒扣在钠的上方(装置如图Ⅰ)。该方案的不足之处有_____________。
Ⅱ.乙同学所采用的装置如图Ⅱ,回答下列问题:
(1)按图Ⅱ组装仪器、添加药品,实验开始后,先将浓盐酸挤入试管,试管中发生反应的离子方程式为;待整套装置中后,点燃酒精灯。
(2)点燃酒精灯后,玻璃管中出现的现象是。
(3)乙同学欲将虚框内装置改为图Ⅲ所示装置,并测量多余气体的体积。
①为提高测量的准确性,图Ⅲ量气管装置中的液体可用;收集完气体后并读数,读数前应进行的操作是冷却至室温并。
②若未冷却至室温立即按上述操作读数,则会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)
③ 如果开始读数时操作正确,最后读数时俯视右边量气管液面,会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)。
I、“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验。因其具有许多优点,已被广泛应用于化学实验中。下图甲是对课本有关Na2O2某性质的两个实验的改进。
(1)将胶头滴管中的水滴入小试管,然后在导管口A、B处分别进行适当操作,再根据所观察现象可得到的两个结论是,。
(2)写出甲中反应的离子方程式。
Ⅱ、Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与H2能反应。为了验证此猜想,该小组同学进行如下实验,实验步骤和现象如下。
步骤1:按图乙组装仪器(图中夹持仪器省略),检查气密性,装入药品;
步骤2:打开K1、K2,产生的氢气流经装有Na2O2的硬质玻璃管,一段时间后,没有任何现象;
步骤3:检验H2的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末变成了白色固体,干燥管内硫酸铜未变蓝色;
步骤4:反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1。
①盛装稀盐酸的仪器名称;B装置的作用是。
②必须检验氢气纯度的原因是。③设置装置D的目的是。
④你得到的结论是(若能反应请用化学方程式表示)。
氢化钙(CaH2)固体是登山运动员常用的能源提供剂。氢化钙要密封保存,一旦接触到水就发生反应生成氢氧化钙和氢气。氢化钙通常用氢气与金属钙加热制取,图1是模拟制取装置。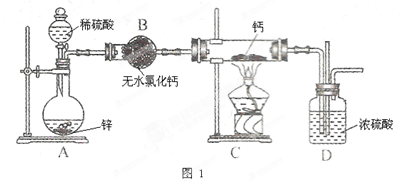
(1)装置B的作用是;
写出装置A中发生的反应的离子方程式。
试用双线桥分析氢化钙与水的反应。
(2)利用图1实验装置进行实验,实验步骤如下:检查装置气密性后装入药品;打开分液漏斗活塞,(请按正确的顺序填入下列步骤的序号)。
①加热反应一段时间②收集气体并检验其纯度
③关闭分液漏斗活塞④停止加热,充分冷却
(3)甲同学设计一个实验,测定上述实验中得到的氢化钙的纯度。请完善下列实验步骤。 ①样品称量②加入__ ______溶液(填化学式),搅拌、过滤③________(填操作名称) ④_______(填操作名称)⑤称量碳酸钙的质量
为了探究HClO的漂白性,某同学设计了如下的实验。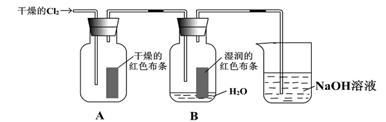
(1)写出C12与水反应的化学方程式________________________
(2)通入C12后,集气瓶A中的现象是__________________,集气瓶B中的现象是_______________,可得出的结论是___________________________。烧杯中的NAOH溶液的作用是,其反生反应的离子方程式为
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题: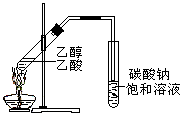
(1)写出制取乙酸乙酯的化学反应方程式,并指出其反应类型:_____ ,属于_______________反应。
(2)浓硫酸的作用是:①_________________________;②____________________。
(3)装置中通蒸气的导管要插在_____________溶液的液面上,不能插入溶液中,目的是防止_______ 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是___________。
A.蒸馏 B.分液 C.过滤 D.结晶
(5)用30克乙酸与46克乙醇反应,如果实际产率是理论产率的67%,则可得到乙酸乙酯的质量是______________。
A.29.5克 B.44克 C.74.8克 D.88克