已知
H2(g)+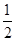 O2(g)===H2O(g) ΔH=a kJ·mol-1
O2(g)===H2O(g) ΔH=a kJ·mol-1
H2(g)+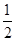 O2(g)===H2O(l) ΔH=b kJ·mol-1
O2(g)===H2O(l) ΔH=b kJ·mol-1
C(s)+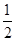 O2(g)===CO(g) ΔH=c kJ·mol-1
O2(g)===CO(g) ΔH=c kJ·mol-1
C(s)+H2O(g) = CO(g) +H2(g) ΔH=d kJ·mol-1
下列关于上述反应焓变的判断正确的是
| A.a>0,c<0 | B.b<0,d<0 |
| C.a>b | D.d=c-b |
溶质的质量分数为a,溶质的物质的量浓度为c mol/L的NaCl溶液,蒸发溶剂,恢复到原来温度,若溶质的质量分数变为2a,则溶质的物质的量浓度变为()
| A.大于2c mol/L | B.小于2c mol/L |
| C.等于2c mol/L | D.在c mol/L和2c mol/L之间 |
下列反应对应的离子方程式中正确的是()
A.铜与浓硝酸混合:Cu+4HNO3(浓)====Cu2++2 +2NO2↑+2H2O +2NO2↑+2H2O |
B.用惰性电极电解MgCl2溶液:2Cl-+2H2O Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.NaHSO4溶液与Ba(OH)2溶液混合呈中性: +Ba2++2OH-====BaSO4↓+ +2H2O |
| D.氢氧化铜溶于氢溴酸:Cu(OH)2+2H+====Cu2++2H2O |
下列说法中正确的是 ()
()
| A.金属氧化物一定是碱性氧化物,非金属氧化物一定是酸性氧化物 |
| B.难溶于水的电解质一定是弱电解质 |
| C.离子化合物中可能含有共价键 |
| D.由同种元素组成的物质一定属于纯净物 |
设NA代表阿伏加德罗常数的数值,下列说法中正确的是 ( )
①常温常压下,17 g甲基(-14CH3)所含的中子数为9NA
②常温常压下,22.4 L NO气体的分子数小于NA
③64 g铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100 mL 0.5 mol/L的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标准状况下,22.4 L二氯甲烷所含有的分子数为NA
⑥常温常压下,1 mol氦气含有的核外电子数为4NA
| A.①② | B.③④ | C.②④ | D.⑤⑥ |
下列溶液中氯离子浓度最大的是()
| A.2mol/L 500mLMgCl2溶液 | B.2.5mol/L 1000mLNaCl溶液 |
| C.1mol/L 250mLAlCl3溶液 | D.5mol/L 300mLKClO3溶液 |