向CuSO4溶液中逐滴加入 KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通人SO2气体,溶液逐渐变成无色。下列分析正确的是
| A.滴加KI溶液时,转移2mol e-时生成1mol白色沉淀 |
| B.通入S2后溶液逐渐变成无色,体现了SO2的漂白性 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
| A.蒸馏、蒸发、萃取、过滤 | B.蒸馏、过滤、萃取、蒸发 |
| C.萃取、过滤、蒸馏、蒸发 | D.过滤、蒸发、萃取、蒸馏 |
下列关于Fe(OH)3胶体的制备,正确的操作是
| A.将FeCl3 溶液滴入蒸馏水中即可 |
| B.将FeCl3 溶液滴入热水中,得到黄色液体即可 |
| C.将FeCl3 溶液滴入沸水中,得到红褐色液体即可 |
| D.将FeCl3 溶液滴入沸水中,并继续加热煮沸至生成红褐色沉淀即可 |
下列不属于置换反应的是
A.CuO+H2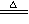 Cu+H2O Cu+H2O |
B.C+2CuO 2Cu+CO2 2Cu+CO2 |
C.Fe2O3+3CO2 Fe+CO2 Fe+CO2 |
D.Fe+CuSO=FeSO+Cu |
将30 mL 0.5mol/L的NaOH溶液加水稀释到500 mL,稀释后NaOH的物质的量浓度为
| A.0.3 mol/L | B.0.03 mol/L | C.0.05 mol/L | D.0.04 mol/L |
需要垫上石棉网加热的仪器是
| A.试管 | B.圆底烧瓶 | C.坩埚 | D.蒸发皿 |