【改编】现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,一定条件下存在反应:H2(g) + I2(g) 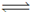 2HI(g) ΔH<0,恒容条件下在Ⅰ中充入1 mol H2和1 mol I2(g),恒压条件下在Ⅱ中充入2 mol HI(g) ,绝热条件下在Ⅲ中充入2 mol HI(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是
2HI(g) ΔH<0,恒容条件下在Ⅰ中充入1 mol H2和1 mol I2(g),恒压条件下在Ⅱ中充入2 mol HI(g) ,绝热条件下在Ⅲ中充入2 mol HI(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是
| A.容器Ⅰ、Ⅱ中达平衡所需时间相同 |
| B.容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C.平衡时容器Ⅱ中c(I2)小于容器Ⅲ中的c(I2) |
| D.容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1 |
下列关于有机化学发展史的说法错误的是网]
| A.中国科学家成功合成了结晶牛胰岛素,标志着人类合成蛋白质时代的开始 |
| B.德国化学家李比希提出运用同位素示踪法研究化学反应历程 |
| C.瑞典科学家贝采利乌斯提出有机化学的概念,使之成为化学的一个重要分支 |
| D.德国化学家维勒用氰酸铵合成尿素,从而打破了无机物和有机物的界限 |
自然界中化合物的种类最多的是
| A.无机化合物 | B.有机化合物 | C.铁的化合物 | D.碳水化合物 |
有机化学主要研究有机化合物所发生的反应,下列化合物中不是有机物的是
| A.CO2 | B.C2H6 | C.HCHO | D.CH3OH |
将51.2gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4,NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为: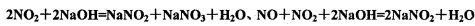 。则生成
。则生成
的盐溶液中NaNO3的物质的量为
| A.0.4 mol | B.0.2 mol | C.0.6 mol | D.0.8 mol |
右表是元素周期表中短周期的一部分,已知A元素的原子中最外层电子数是其电子层数的3倍。下列关于表中六祌元素的说法不正确的是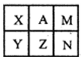
| A. X元素形成的气态氢化物分子空间结构呈三角锥形 |
| B. X、Y、Z三种元素形成的单核阴离子半径中Y最大 |
| C.X的氢化物分子间存在氢键,因此X的熔沸点较高 |
| D.最高价氧化物对应的水化物酸性最强的元素是M元素 |