下列说法正确的是
A.0.01mol/L的Na2HPO4溶液中存在如下的平衡:HPO42-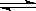 H++PO43-,加水稀释,使溶液中的HPO42-、H+、PO43-的浓度均减小 H++PO43-,加水稀释,使溶液中的HPO42-、H+、PO43-的浓度均减小 |
| B.饱和NH4Cl溶液中:c(H+)+c(Cl-)=c(NH4+)+2c(NH3•H2O)+c(OH-) |
| C.常温下,0.01mol/L的 HA和BOH两种溶液,其pH值分别为3和12,将两溶液等体积混和后,所得溶液的pH≤7 |
| D.在NH4HSO3与NH4Cl混合溶液中,c(NH4+)= c(SO32-)+ c(HSO3-)+ c(H2SO3)+ c(Cl-) |
下列离子方程式书写正确的是()
| A.金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑ |
| B.碳酸钡中加入过量盐酸:CO32-+2H+=CO2↑+H2O |
| C.偏酸铝钠溶液中加入过量盐酸:AlO2-+4H+=Al3++2H2O |
| D.铁粉加入到FeCl3溶液中:Fe+Fe3+="2" Fe2+ |
若NA代表阿伏加德罗常数的值,以下说法正确的是()
| A.3.6g重水含有的电子数为2NA |
| B.常温常压下,22.4升氯气所含的原子数目为2NA |
| C.常温常压下,活泼金属从盐酸中置换出1mol H2,发生转移的电子数为2NA |
| D.在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为2NA |
下列实验设计和结论相对应的是()
| A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| C.某无色溶液中滴加Ba(NO3)2溶液,产生白色沉淀,则原溶液中一定有SO42- |
| D.某气体能使澄清石灰水变浑浊,该气体一定是CO2 |
下列关于常见有机物的说法正确的是()
| A.乙烯和苯都能与溴水反应 |
| B.苯只能发生取代反应,不能发生加成反应 |
| C.糖类、油脂、蛋白质都能发生水解反应 |
| D.乙酸和油脂都能与氢氧化钠溶液反应 |
向浓盐酸中加入浓H2SO4时,会有白雾生成,不属于产生该现象的原因是()
| A.浓盐酸具有还原性 | B.浓盐酸具有挥发性 |
| C.浓H2SO4具有吸水性 | D.气体溶质的溶解度随温度升高而降低 |