实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250 mL溶液。
方案一:沉淀法。利用化学反应把HCO3—、CO32—完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中ω(Na2CO3)。
(1)量取100 mL配制好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO3—、CO32—完全转化为沉淀,应选用的试剂是 (填编号)。
| A.CaCl2溶液 | B.MgSO4溶液 | C.NaCl溶液 | D.Ba(OH)2溶液 |
(2)过滤,提取沉淀,则过滤操作所需要的玻璃仪器除烧杯外,还有 。
(3)将沉淀洗涤,并充分干燥,称量沉淀的质量为mg,由此可以计算(Na2CO3)。如果此步中,沉淀未干燥充分就称量,则测得ω(Na2CO3) (填“偏大”、“偏小"或“无影响")。
方案二:量气法。量取10.00 mL配制好的溶液与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃、1.01×105 Pa)的体积,由此计算混合物中W(Na2CO3)。
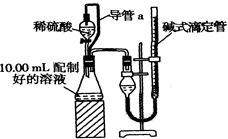
(1)装置中导管a的作用是 。若撤去导管a,使测得气体体积 (“偏大”,“偏小”或“无影响”)
(2)反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
① ,② ,③眼睛视线与液面最低处相平。
(3)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生CO2的体积为 ml。
方案三:滴定法。量取25.00 mL配制好的溶液加入锥形瓶中,滴加2滴酚酞试剂,摇匀,用0.2000 mol/L的盐酸滴定到终点(已知终点时反应H++CO32—=HCO3—恰好完全)。重复此操作2次,消耗盐酸的体积平均值为20.00 mL。
(1)量取25.00 mL配制好的溶液,应选择 仪器来完成。
(2)判断滴定终点的依据是 。
(3)此法测得ω(Na2CO3)= %。
测定水中溶液氧气的方法是:取a mL水样,迅速加入MnSO4溶液及含有NaOH的KI溶液,立即塞上塞子、振荡,使之充分反应;打开塞子,迅速加入适量的稀硫酸,此时有I2生成;再用Na2S2O3溶液(浓度b mol/L)和I2反应,消耗了VmL达到终点(以淀粉作指示剂)。有关方程式为:①2Mn2++O2+4OH-=2MnO(OH)2(反应很快);②MnO(OH)2+2I-+4H+=Mn2++I2+3H2O;③I2+2S2O32-=S4O62-+2I-。
⑴需要进行滴定的反应是,终点的颜色变化为。
⑵将Na2S2O3溶液盛放在(“酸式”或“碱式”)滴定管中。
⑶在加入MnSO4溶液及含有NaOH的KI溶液和适量的稀硫酸时,要迅速的加入,否则将对结果造成(“偏高”、“偏低”或“无影响”),原因是
。
⑷在加入MnSO4溶液及含有NaOH的KI溶液振荡时,塞子未塞紧,溅出部分溶液,则将对结果造成(“偏高”、“偏低”或“无影响”),原因是
。
⑸水中溶液O2为(以m g/L为单位)。
从环己烷可制备1,4-环己二醇的二醋酸酯,下列有关的8步反应(其中所有无机产物都已略去):
其中有3步属于取代反应,2步属于消去反应,3步属于加成反应。
反应①____和____属于取代反应。
化合物的结构简式是:B____,C_____。
反应④所用试剂和条件是_______。
向碳酸钠的浓溶液中逐滴加入稀盐酸,直到不再生成二氧化碳气体为止,则在此过程中,溶液中的碳酸氢根离子浓度变化趋势可能是:
| A.逐渐减小; | B.逐渐增大; | C.先逐渐增大,而后减小; | D.先逐渐减小,而后增大。你的选择是____(填正确选项的标号)。试用化学方程式和简要文字表达其理由。____________________ |
某种混合气体,可能含有N2、HCl、CO。把混合气体依次通过足量的NaHCO3溶液和灼热CuO,气体体积都没有变化。再通过足量的NaO2固体,气体体积减小。最后通过灼热的铜网,经充分反应后气体体积又减小,但还有剩余气体。以下对混合气体组成的判断,正确的是
| A.一定没有N2;CO和HCl中至少有一种 |
| B.一定有N2、HCl和CO |
| C.一定有N2;CO和HCl中至少有一种 |
| D.一定有N2和HCl;没有CO |
碳和硅的性质相似。碳的最简单的氢化物是甲烷,硅的最简单的氢化物称为甲硅烷(SiH4)。甲硅烷是一种无色无味的气体(其密度比空气大),不易溶于水,其化学性质比甲烷活泼。在实验室里制取甲硅烷的方法是:将白净细沙(SiO2)与镁粉混合起来,灼烧到反应物转变为灰黑色的硅化镁(Mg2Si)和白色的氧化镁后冷到室温;取一定量的灼烧后的残留物,置于制取甲硅烷的装置中,滴加稀盐酸后立即有甲硅烷气体逸出,并迅速地自燃。
(1)写出以上叙述中涉及的化学方程式:
①____________________________________________________________
②____________________________________________________________
③____________________________________________________________
④____________________________________________________________。
(2)制取甲硅烷的装置与制取__________ (填“H2”或“O2”)的装置相似。
(3)加入稀盐酸之前后应向密闭装置中通入氮气一会儿,其目的是__________。
(4)为研究甲硅烷的化学性质,进行了如下实验:
①将甲硅烷通入少量的硝酸银溶液中,发现有沉淀生成,后经测定知该沉淀为混合物,其中有二氧化硅。向充分反应后的溶液中滴入几滴稀盐酸,未发现有白色沉淀。向反应后的原溶液中滴入几滴碳酸钠溶液,却发现有气泡迅速放出。将甲硅烷通入硝酸银溶液中发生反应的化学方程式为___________________________________________________________________。
②制取甲硅烷后,检验装置中是否有残留的的甲硅烷的方法是__________________________。