已知AgCl、AgBr的溶解度分别为1.5×10-4g、8.4×10-6 g(20℃)。将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓硝酸银溶液,发生的反应为
| A.只有AgBr沉淀生成 | B.AgCl和AgBr沉淀等量生成 |
| C.AgCl沉淀少于AgBr沉淀 | D.AgCl沉淀多于AgBr沉淀 |
已知H2(g)+Br2(l)="2HBr(g)" △H=-72kJ/mol,蒸发1mol 液溴变Br2(g)需要吸收的能量为30kJ,其它相关数据如下表:()
| H2(g) |
B r2(g) r2(g) |
HBr(g) |
|
| 1mol分子中的化学键断裂时需要吸收的能量/kJ |
436 |
a |
369 |
则表中a为
| A.404 | B.260 |
| C.230 | D.200 |
下列生活中现象与盐类水解无关的是( )
| A.NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂 |
| B.草木灰与铵态氮肥不能混合施用 |
| C.粗盐在空气中易潮解 |
| D.用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
下列有关化学反应速率的说法正确的是( )
| A.凡是能量达到活化能的分子发生的碰撞均为有效碰撞。 |
| B.增大反应物浓度能加快正反应的反应速率,降低逆反应的反应速率 |
| C.温度升高使化学反应速率加快的主要原因是增加了反应物分子之间的碰撞次数 |
| D.决定化学反应速率的根本因素是参加反应的各物质的性质 |
下列化学方程式中,属于水解反应且正确的是()
A.HCO3-+H2O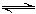 H3O++CO32- H3O++CO32- |
B.CO32-+2H2O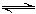 H2CO3+2OH- H2CO3+2OH- |
C.CO32-+H2O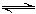 HCO3-+OH- HCO3-+OH- |
D.Cl2+H2O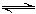 H++ Cl- + HClO H++ Cl- + HClO |
关于中和热测定实验的下列说法不正确的是()
| A.烧杯间填满碎泡沫塑料是减少实验过程中的热量损失 |
| B.使用环形玻璃棒既可以搅拌又避免损坏温度计 |
| C.向盛装酸的烧杯中加碱时要小心缓慢 |
| D.测了酸后的温度计要用水清洗后再测碱的温度 |