氮元素的化合物应用十分广泛。请回答:
(1)火箭燃料液态偏二甲肼(C2H8N2)是用液态N2O4作氧化剂,二者反应放出大量的热,生成无毒、无污染的气体和水。已知室温下,1 g燃料完全燃烧释放出的能量为42.5kJ,则该反应的热化学方程式为 。
(2)298 K时,在2L固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物质的量浓度随时间变化如图。达平衡时,N2O4的浓度为NO2的2倍,回答下列问题:

①298k时,该反应的平衡常数为 L·mol-1(精确到0.01)。
②下列情况不是处于平衡状态的是 :
A.混合气体的密度保持不变;
B.混合气体的颜色不再变化;
C.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)="0.6" moln(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”)。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点。
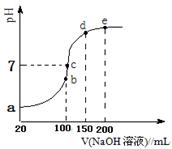
①b点时,溶液中发生水解反应的离子是______;
②在c点,溶液中各离子浓度由大到小的排列顺序 。
③d、e点对应溶液中,水电离程度大小关系是d e(填“>”、“<”或“=”)。
下表是元素周期表的一部分,表中所列字母分别代表短周期中的一种元素:
| A |
B |
||||||
| C |
D |
(1)A单质电子式是;B元素在周期表中的位置是。
(2)D单质与C的最高价氧化物对应水化物反应的离子方程式是。
(3)A的气态氢化物与其最高价氧化物对应水化物反应所得产物的名称是,该产物对水的电离起促进作用的原因是。
(17分)阿魏酸在医药、保健品、化妆品原料和食品添加剂等方面有着广泛的用途,其
结构简式为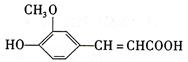
⑴阿魏酸可以发生 (填选项字母)。"
a.酯化反应 b.消去反应 c.加成反应 d.氧化反应 e.银镜反应
⑵阿魏酸的一种同分异构体A 可用于制备有机玻璃(聚甲基丙烯酸甲酯),转化关系如下图所示: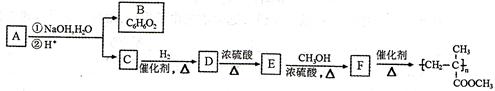
己知A 和B都能与FeCl3溶液发生显色反应,B的一溴代物只有一种,A、C能发生银镜反应。
①B的结构简式为____________,C含有的官能团为____________。
②D→E的化学方程式为____________________________________。
③A的结构简式为__________________________________________。
(3)写出所有符合下列条件的阿魏酸的同分异构体的结构简式。
①苯环上有两个取代基,且苯环上的一漠代物只有2 种;
②能发生银镜反应;
③与碳酸氢钠溶液反应可放出使澄清石灰水变浑浊的气体;
④与FeCl3溶液发生显色反应__________________________________________。
(14 分)在T1℃时,向容积为2 L 的密闭容器甲中加人1mol N1、3mol H2及少量固体催化剂,发生反应N2(g) + 3H2(g)  2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
2NH3(g);△H<0,10min时各物质的浓度不再变化,测得NH3 的体积分数为25% 。
(1) 该反应在0 ~l0min 时间内H2的平均反应速率为______,N2的转化率为______。 (2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
(2)在T1℃时,若起始时在容器甲中加入0.5mol N2、1.5mol H2、0.5mol NH3 ,则达到平衡时NH3的体积分数______ (填选项字母) 。
a.大于25% b.等于25% c.小于25%
(3)右图是在T1℃时密闭容器甲中H2的体积分数随时间t的变化曲线,请在该图中补画出该反应在T2℃(T1>T2)时H2的体积分数随时间t的变化曲线。
(4)若保持T1℃,在体积也为2 L 的密闭容器乙中通入一定量的N2、H2、NH3,欲使平衡时容器乙中各物质的物质的量与容器甲中完全相同,且起始时反应向正反应方向进行,则通入H2的物质的量x的取值范围是____________。
(13分)X、Y、W、Q都是短周期元素,已知Y、X、W、Q的原子半径依次增大,X、Y 同周期,X、W 同主族,W 原子核内的质子数等于X、Y 原子核内的质子数之和,W 原子最外层电子数是Q 原子最外层电子数的3 倍。
(l)写出下列元素符号:X______,Y______,W______,Q________。
(2)W元素的单质有广泛用途,工业上制备该单质的化学方程式为:
______________________________________________________________________。
(3)Y元素的某种单质通大酸性淀粉碘化钾溶液中,溶液变蓝,同时生成Y元素的另一种单质,该反应的离子方程式为:
______________________________________________________________________。
(4)Y、W、Q三种元素可组成一种盐,其溶液中各离子的浓度从大到小的顺序为
______________________________________________________________________。
已知:
物质A在体内脱氢酶的作用下会氧化为有害物质GHB。下图是关于物质A的一种制备方法及由A引发的一系列化学反应。

请回答下列问题:
(1)写出反应类型:反应①,反应②。
(2)写出化合物B的结构简式。
(3)写出反应②的化学方程式。
(4)写出反应④的化学方程式。
(5)反应④中除生成E外,还可能存在一种副产物(含 结构),它的结构简式为。
结构),它的结构简式为。
(6)与化合物E互为同分异构体的物质不可能为(填写字母)。
a、醇 b、醛 c、羧酸 d、酚