【改编】磷酸铁锂电池的电池的内部结构如图所示。左边是磷酸铁锂材料作为电池的正极,由铝箔与电池正极连接,中间是聚合物的隔膜,它把正极与负极隔开,但锂离子Li+可以通过而电子不能通过,右边是由石墨组成的电池负极,由铜箔与电池的负极连接。电池的上下端之间是电池的电解质,电池由金属外壳密闭封装。电池的总反应为: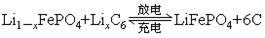

下列关于电池的说法不正确的
| A.磷酸铁锂电池放电时,锂离子从负极中脱离出来,经过电解液,穿过隔膜回到正极材料中 |
| B.放电时负极反应:LixC6-xe- ="=" 6C+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料) |
| C.充电时的阳极反应:LiFePO4 -xe-="=" Li1-xFePO4+xLi+ |
| D.若用该电池电解精炼粗铜,阳极质量减少12.8g 时,则电池中通过聚合物隔膜的Li+数为0.4NA |
海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示。下列说法不正确的是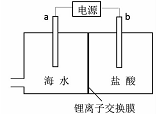
| A.a连接电源的正极 |
| B.Li+的移动方向是从海水进入到盐酸中 |
| C.一段时间后,b电极附近溶液的pH降低 |
| D.电解过程中还可能获得有经济价值的副产物氢气和氯气 |
下列说法不正确的是
| A.银氨溶液可以用于区分麦芽糖和蔗糖 |
| B.乙醇、乙二醇、丙三醇的沸点依次升高 |
C.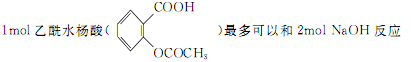 |
D. |
下列叙述中正确的是
| A.根据上图,若滴定前仰视读数,滴定终点时俯视读数,则测定的盐酸浓度偏高 |
| B.25℃时,难溶物XY和AB3的KSP分别为1.0×10-10和2.7×10-15,则饱和溶液中C(X+)一定大于C(A3+) |
| C.每个Fe(OH)3胶体粒子含一个氢氧化铁分子 |
| D.某溶液中存在K+、HCO-3、CO2-3、OH-、H+,其离子浓度大小顺序可能为c(K+)>c(HCO-3)>c(H+)>c(CO32-) |
现有5种短周期元素X、Y、Z、Q、W,原子序数依次增大,在周期表中X原子的半径最小;X和W同主族;Y原子的核外电子总数是其次外层电子数的3倍,Q是地壳中含量最高的元素。下列说法不正确的是
| A.原子半径:Y<Q<W |
| B.ZX3可使紫色石蕊试液变蓝 |
| C.X、Z、Q可组成离子化合物或共价化合物 |
| D.X2Q2、Y2X6两种分子中含有的电子数、化学键种类都相同 |
下列实验装置和试剂的选用或操作都正确的是