工业上常用FeSO4制备Fe2O3,反应方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑,若将生成的气体通入足量的氯化钡和氨水的混合溶液中,得到的沉淀物是
Fe2O3+SO2↑+SO3↑,若将生成的气体通入足量的氯化钡和氨水的混合溶液中,得到的沉淀物是
| A.BaSO3和BaSO4 | B.BaS | C.BaSO3 | D.BaSO4 |
已知C5H11Cl共有8种同分异构体,可推知分子式为C5H12O醇(属醇类)的同分异构体的数目共有()
| A.9种 | B.6 种 | C.5种 | D.8种 |
根据下列反应步骤,由2-丙醇转化为1,2—丙二醇(HOCH2—CHOH—CH3)的正确的反应类型的顺序是()
| A.消去―取代―加成 | B.取代―消去―加成 |
| C.消去―加成―水解 | D.水解―取代―取代 |
只用水就能鉴别的一组物质是 ()
()
| A.苯、乙酸、四氯化碳 | B.乙醇、乙醛、乙酸 |
| C.乙醛、乙二醇、溴乙烷 | D.苯酚、乙醇、甘油[ |
据质谱图分析知某烷烃的相对分子质量为86,其核磁共振氢谱图有4个峰,峰面积比为6:4:3:1,则其结构简式为()
A. |
B.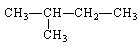 |
C.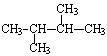 |
D.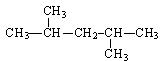 |
下列物质在一定条件下,不能和H2发生加成反应的是()
| A.CH3CH2CHO | B.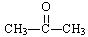 |
C.CH2 ="CHCOOH" | D.CH3COOH |