把aL含硫酸铵、硝酸铵的溶液分成两等份,一份用b mol烧碱刚好把NH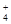 转化为NH3,另一份与氯化钡溶液完全反应消耗c mol BaCl2。则原溶液中NO
转化为NH3,另一份与氯化钡溶液完全反应消耗c mol BaCl2。则原溶液中NO 的浓度为
的浓度为
A.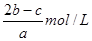 |
B.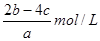 |
C.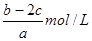 |
D.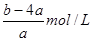 |
下列离子能够大量共存,且满足相应要求的是
| 选项 |
离 子 |
要 求 |
| A |
NH、Al3+、SO、H+ |
滴加NaOH溶液立刻有气体产生 |
| B |
K+、NO、Cl-、HS- |
c(K+)<c(Cl-) |
| C |
Fe2+、NO、SO、Cl- |
逐滴滴加盐酸时溶液没有颜色变化 |
| D |
Na+、HCO、Mg2+、SO |
滴加氨水立即有沉淀产生 |
下列离子方程式书写正确的是
| A.硫氢化钠的水解:HS-+H2O === S2-+H3O+ |
| B.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=== Fe3++3H2O |
| C.钢铁发生吸氧腐蚀的负极反应式:O2+4e-+2H2O === 4OH- |
| D.碳酸氢铵溶液中滴入少量烧碱溶液:HCO3-+OH-=== CO32-+H2O |
下列说法中错误的是
| A.0.5 L 2 mol·L-1 AlCl3溶液中,Al3+和Cl-总数小于4×6.02×1023个 |
| B.制成0.5 L 10 mol·L-1的盐酸,需要标准状况下的氯化氢气体112 L |
| C.从1 L 1 mol·L-1的NaCl溶液中移取出10 mL溶液,其浓度是1 mol·L-1 |
| D.10 g 98%的硫酸(密度为1.84 g·cm-3)与10 mL18.4 mol·L-1的硫酸的浓度不同 |
NA表示阿伏加德罗常数,下列判断正确的是
| A.标准状况下22.4 L的CCl4中含有NA个分子 |
| B.1 mol Cl2溶于足量水中一定转移NA个电子 |
| C.18 g 18O2和18O3中一共含有NA个18O原子 |
| D.1 mol·L-1的NaOH溶液中共含有NA个Na+ |
加碘盐的主要成分是NaCl,还添加了适量的KIO3。下列说法中正确的是
| A.KIO3和NaCl为离子化合物,均只含离子键 |
B.KIO3中阳离子的结构示意图为 |
| C.23Na37Cl中质子数和中子数之比是8∶7 |
| D.次碘酸的结构式为H—O—I |