将钠、钾分别投入相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为()
A.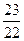 ∶ ∶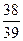 |
B.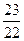 ∶ ∶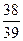 |
C.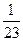 ∶ ∶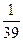 |
D.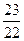 ∶ ∶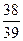 |
下列说法中符合碱金属特点的是()
| A.碱金属的盐都有焰色反应,而其单质及其氧化物则没有 |
| B.碱金属的单质及合金在通常情况下都是固体 |
| C.碱金属氧化物都是碱性氧化物,都易溶于水 |
| D.碱金属的绝大部分盐都是易溶于水的 |
焰色反应属于()
| A.元素的性质 | B.单质的性质 |
| C.离子的性质 | D.化合物的性质 |
按Li、Na、K、Rb、Cs的顺序依次递减的性质是()
| A.元素的金属性 | B.单质的还原性 |
| C.单质的熔点 | D.单质的密度 |
氢化锂(LiH)是一种离子化合物,它与水反应生成H2。以下叙述正确的是()
A水溶液呈酸性 B.H-与He的核外电子排布相同
C.H-可以被还原成氢气 D.H2O在反应中作氧化剂