已知反应:2SO2(g)+O2(g)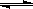 2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g) ΔH<0.某温度下,将2 mol SO2和1 mol O2置于 10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是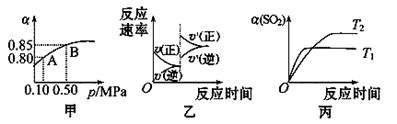
| A.由图甲知,B点SO2的平衡浓度为0.3mol·L-1 |
| B.由图甲知,A点对应温度下的平衡常数为80 |
| C.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
| D.达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示 |
将等物质的量的镁和铝相混合,取等质量的该混合物四份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )。
| A.3 mol·L-1 HCl溶液 | B.4 mol·L-1 HNO3溶液 |
| C.8 mol·L-1 NaOH溶液 | D.18 mol·L-1 H2SO4溶液 |
用铝热法还原下列化合物,制得金属各1 mol时,消耗铝最少的是( )。
| A.MnO2 | B.WO3 | C.Co3O4 | D.CrO3 |
下列说法错误的是( )。
| A.对废旧金属的最好处理方法是回收、再利用 |
| B.提炼金属要经过矿石的富集、冶炼、精炼三步 |
| C.活泼金属的冶炼都是通过电解其盐溶液制得 |
| D.热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等 |
南极考察队在印度洋发现了一种不寻常的鱼,它的血液像水一样无色透明。研究发现这种鱼的血液中某种元素的含量是其他鱼的血液中的十分之一。这种元素最有可能是( )。
| A.Cu | B.Ag | C.Fe | D.Pb |
随着人们生活质量地不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是( )。
| A.利用电池外壳的金属材料 | B.防止电池造成污染 |
| C.废电池经过处理后还可以重新使用 | D.回收其中的非金属材料 |