【化学---物质结构与性质】物质结构决定物质的性质,物质的性质反映物质结构。
(1)BCl3、NCl3发生水解反应化学方程式如下:
BCl3+ 3 H2O = B(OH)3 + 3 HCl
NCl3+ 3 H2O = NH3 +3 HClO
分析上述反应,判断B、N、Cl三种元素的电负性由大到小的顺序是____________________。上述反应所含的微粒中,呈三角锥形的是_____________(填化学式)。
(2)BN是一种新型无机非金属材料,熔点很高、硬度很大,晶胞结构如图所示。BN晶体中存在的作用力有____(填字母编号)。
A.σ键 B.π键 C.配位键 D.分子间作用力
(3)B(OH)3晶体结构如图所示。晶体中B原子的轨道杂化方式是______________;B(OH)3可能具有的性质是_______(填字母编号)。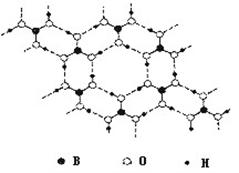
A.熔化状态下能导电 B.熔点很高
C.能形成[B(OH)4]— D.硬度很大
(4)还原铁粉可作为合成氨的触媒。基态Fe原子的核外有________个未成对电子。从原子结构的角度分析,二价铁易被氧化为三价铁的原因是___________________________。
取3.320g只含羧基,不含其它官能团的固态芳香族羧酸置于4L氧气中,经点燃,羧酸完全燃烧,反应后气体体积增加了0.224L,将气体通过足量的固体Na2O2后,体积减少1.792L(所有体积均在标准状况下测定)。请回答:
(1)3.320g该羧酸中碳元素的物质的量为_______________mol。
(2)该羧酸中C、H、O的原子个数比为____________________。
(3)写出符合以上各条件的相对分子质量最小的芳香族羧酸的结构简式__________。
0.1mol CmHnCOOH与Br2完全加成时需Br2 16g,0.1mol该有机物完全燃烧时产生CO2和H2O的物质的量之和为3.5mol,试通过计算确定该有机酸的结构简式。
)由若干种可溶性物质组成的固体混合物X,可能含有的阳、阴离子分别是:
| 阳离子 |
Na+、Mg2+、Al3+、Ag+、Ba2+ |
| 阴离子 |
OH-、Cl-、SO42-、SO32—、CO32- |
为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
(1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是__________________。
(2)向溶液中滴加盐酸溶液。刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则X中一定存在的离子是____________________,一定不存在的离子有____________________。
(3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可)____________。
(4)尚待检验的离子及检验方法是:
| 尚待检验的离子 |
检验方法 |
已知:氧化性:KMnO4>HNO3;Bi 元素+3价较稳定,Na3BiO3溶液为无色。取一定量的Mn(NO3)2溶液依次进行下列实验,现象记录如下。
①滴加适量的Na3BiO3溶液,溶液变为紫红色。
②继续滴加适量H2O2,紫红色褪去,并有气泡产生。
③再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
④最后通入足量的SO2气体,请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为___________________________;
(2)实验④中的现象为:________________________________________________;
(3)实验②反应的离子方程式是:
__________________________________________________________________;
(4)实验③反应的离子方程式是:________________________________________。
有机物A相对分子质量为100,1mol A充分燃烧后只生成4mol CO2和2mol H2O,该有机物有如下转化关系:
试回答:
(1)1mol A与2mol H2反应生成1mol E,其反应方程式是______________________。
(2)与A具有相同官能团的A的同分异构体的结构简式是______________________。
(3)B酸化后与Br2反应得到D,其反应类型是______________________。
(4)F的结构简式是_____________________。