用酸性氢氧燃料电池(甲池)为电源进行电解的实验装置(乙池,一定条件下可实现有机物的电化学储氢)如下图所示.甲池中C为含苯的物质的量分数为10%的混合气体,D为l0mol混合气体其中苯的物质的量分数为24%(杂质不参与反应),E为标准状况下2. 8mol气体(忽略水蒸汽),下列说法正确的是
| A.甲池中A处通入H2,E处有O2放出 |
| B.甲池中H+由F极移向G极 |
| C.乙池中阴极区只有苯被还原 |
| D.导线中共传导11.2mol电子 |
CO2气体在一定条件下可与金属镁反应,干冰在一定条件下可以形成CO2气体,这两个变化过程中需要克服的作用分别是
| A.共价键,共价键 | B.共价键,分子间作用力 |
| C.分子间作用力,共价键 | D.分子间作用力,分子间作用力 |
下列事实能说明氯的非金属性比硫强的是
| A.次氯酸的酸性比硫酸弱 |
| B.氯气能置换氢硫酸(H2S的水溶液)中的硫 |
| C.氢硫酸是弱酸,而盐酸是强酸 |
| D.硫在常温下为固态,而氯气为气态 |
依据元素周期表及元素周期律,下列推断正确的是
| A.H3BO3的酸性比H2CO3的强 |
| B.Mg(OH)2的碱性比Be(OH)2的强 |
| C.HCl、HBr、HI的热稳定性依次增强 |
| D.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
根据下列性质判断,属于原子晶体的物质是
| A.熔点2 700 ℃,导电性好,延展性强 |
| B.无色晶体,熔点3 500 ℃,不导电,质硬,难溶于水和有机溶剂 |
| C.无色晶体,能溶于水,质硬而脆,熔点800 ℃,熔化时能导电 |
| D.熔点-56.6 ℃,微溶于水,硬度小,固态或液态时不导电 |
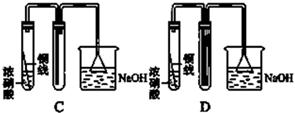
下列装置中,用中间的试管收集浓硝酸和铜反应所生成的气体,最终可使收集到的气体中空气的含量最少的是