图像能直观地反映有关物理量的变化及规律,下列各图像与描述相符的是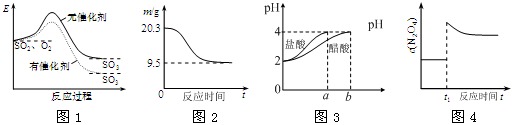
| A.图1表示SO2氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图2表示0.1 mol MgCl2·6H2O在空气中充分加热时固体质量随时间的变化 |
| C.图3表示分别稀释10 mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>100 |
D.图4表示平衡2NO2(g) N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 |
金属冶炼中不会涉及到的反应类型是()
| A.氧化还原反应 | B.置换反应 | C.分解反应 | D.复分解反应 |
诗句“春蚕到死丝方尽,蜡烛成灰泪始干”中“丝”和“泪”分别是()
| A.纤维素、脂肪 | B.淀粉、油脂 | C.蛋白质、高级烃 | D.蛋白质、水 |
许多国家十分重视海水资源的综合利用。下列物质不需要化学变化就能够从海水中获得的是()
| A.氯、溴、碘 | B.钠、镁、铝 | C.烧碱、氢气 | D.食盐、淡水 |
将40 mL 1.5 mol·L-1的CuSO4溶液与 30 mL 3 mol· L-1的NaOH溶液混合,生成浅蓝色沉淀,假如溶液中[Cu2+]或[OH-]都已变得很小,可忽略,则生成沉淀的组成可表示为()
| A. Cu (OH)2 | B. CuSO4·Cu (OH)2 |
| C. CuSO4·2Cu (OH)2 | D. CuSO4·3Cu (OH)2 |
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是()
| A.NaOH | B.NH3·H2O | C.AgNO3 | D.BaCl2 |