(10分)硫铁矿烧渣是一种重要的化工生产中间产物,主要成分是Fe3O4、Fe2O3、FeO和二氧化硅等。下面是以硫铁矿烧渣制备高效净水剂聚合硫酸铁的流程图: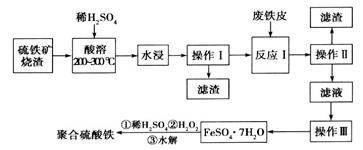
(1)实验室实现“操作I”所用的玻璃仪器有_______、________和烧杯。
(2)检验“酸溶”后的溶液中含有Fe2+试剂是_______,现象是_______。
(3)“操作III”系列操作名称依次为______、______、过滤和洗涤。洗涤的方法是______________。
(4)加入适量H2O2的目的是氧化Fe2+,写出H2O2氧化Fe2+为Fe3+的离子方程式:__________________。
兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
(1)SO2气体还原Fe3+的产物是________(填离子符号),参加反应的SO2和Fe3+的物质的量之比是________。
(2)下列实验方案适用于在实验室制取所需SO2的是________。
A.Na2SO3溶液与HNO3B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(3)装置C的作用是________________________________________________。
(4)若要从A中所得溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有________(填序号)。
A.蒸发皿
B.石棉网
C.漏斗
D.烧杯
E.玻璃棒
F.坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是________,原因是________________________________
(6)能表明I-还原性弱于SO2的现象是________________________________
为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
【探究一】
(1)常温下,工业上用铁质容器盛放冷的浓硫酸,其原因是 。
(2)称取碳素钢6.0g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用 (选填序号)。a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此可求算气体Y中SO2的体积分数。
写出探究②中出现的所有离子反应方程式 。
【探究二】
根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893g·L-1。为此设计了下列探究实验装置(图中夹持仪器省略,假设有关气体完全反应)。
(3)装置B中试剂的作用是 。
(4)分析Y气体中的Q2气体是如何生成的 。(用化学方程式表示)。
(5)为确认Q2的存在,需在装置中添加洗气瓶M于 (选填序号)。
a.A之前 b.A-B间c.B-C间d.C-D间
(6)如果气体Y中含有Q1,预计实验现象应是 。
(14分)海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:
(1)指出提取碘的过程中有关的实验操作名称:① ,② 。
(2)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。
实验控制在较低温度下进行的原因是 ;锥形瓶里发生反应的离子方程式为
(3)在第②步操作过程中,可加入的有关试剂是 。
| A.酒精 | B.四氯化碳 | C.醋酸 | D.苯 |
(4)含碘离子的溶液也可以采用下图方法得到碘
①加入NaNO2并调节pH<4,反应的离子方程式 __________________。
②流程中生成的NO尾气有毒,工业上将其与O2按一定比例通入NaOH制备NaNO2,
写出反应的化学方程式: ____________________。
(5)要测量含碘离子的溶液中I-的浓度,取25 mL该溶液,先加几滴KSCN溶液,再逐滴滴入0.1 mol·L-1FeCl3溶液, 若消耗FeCl3溶液20.4 mL,则含碘离子的溶液中I-的浓度为 。(保留两位有效数字)
现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置:
Ⅰ.探究该合金的某些性质:
(1)取a g合金粉末放入蒸馏烧瓶,并加入足量浓硫酸,A、B中均无明显现象,原因是_________________________________________________________________。
(2)点燃酒精灯一段时间后,A中剧烈反应,请写出A中反应的化学方程式:
________________________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其分成两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应的位置。
| 滴加的溶液 |
氯水 |
氨水 |
| 沉淀的化学式 |
Ⅱ.测定样品中碳的质量分数:
(4)装置F的作用是_______________________________________________________。
(5)反应结束后,若U形管E增重m g,则合金中碳的质量分数为________(用含m和a的式子表示)。若没有装置D,会使合金中碳的质量分数______ (填偏高、偏低、无影响)
(6)若将SO2气体通入含有n mol Na2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体________mol(不考虑溶解的SO2)。
硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境。某化学兴趣小组对废气A的组成进行探究,请回答下列问题。
(1)同学甲设计实验检验废气A中含有的CO2,应选择的试剂有 。
| A.NaOH溶液 | B.酸性KMnO4溶液 | C.澄清石灰水 | D.盐酸 |
(2)同学乙欲测定废气A中SO2的含量,取a L废气A并设计了如下装置进行实验。
①为了保证实验成功,装置A应具有的现象是 ,搅拌的目的是 。
②同学丙认为A装置前后的质量差就是a L废气中含有的SO2的质量,然后进行含量计算。经小组讨论后,同学丁提出疑问,按照同学丙的实验,若废气中SO2完全被吸收,则最后测定的结果应该偏大,同学丁推断的理由是 。
(3)兴趣小组的同学查阅资料发现可利用硫酸工业废气A制备皓矾(ZnSO4•7H2O)。实验模拟制备皓矾工业流程如下:
①“氧化”中加入硫酸铁发生反应的离子方程式是 。
②加入Zn粉的目的是 。
③固体A主要成分是 。