在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH  CH3COO-+H+ ΔH>0。
CH3COO-+H+ ΔH>0。
(1)下列方法中,可以使0.10 mol·L-1 CH3COOH的电离程度增大的是 。
a.加入少量0.10 mol·L-1的稀盐酸
b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1
d.加入少量冰醋酸
e.加入少量氯化钠固体
f.加入少量0.10 mol·L-1的NaOH溶液
(2)pH值相同的 ①HCl(aq)、②H2SO4(aq)、③CH3COOH(aq)各100 mL分别用0.1 mol/L的NaOH(aq)中和,消耗NaOH(aq)的体积分别为V1、V2、V3,它们由大到小的顺序是 。
(3)物质的量浓度相同的①HCl(aq)、②H2SO4(aq)、③CH3COOH(aq)各100mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是 。
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标况下,11.2L SO3所含的分子数目为0.5 NA |
| B.室温下,1L pH=1的稀硫酸溶液中,由水电离的H+离子数目为0.2NA |
| C.铅蓄电池放电时,正极消耗4mol H+,则电路中通过的电子数目为2NA |
| D.8 Al + 3NH4ClO4 ="4" Al2O3 +3NH3 +3HCl 反应中,消耗27gAl粉时,转移的电子数目为2.75NA(Al原子量—27) |
能在水溶液中大量共存的一组离子是
| A.H+、Fe3+、I-、SO42- | B.Al3+、Mg2+、CO32-、Cl- |
| C.K+、Ag+、Ca2+、NO3- | D.NH4+、Na+、OH-、MnO4- |
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是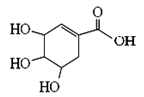
| A.分子式为C7H6O5 | B.分子中含有两种官能团 |
| C.可发生加成和取代反应 | D.分子中有7个碳原子共平面 |
(共7分)(1)0.5 mol H2SO4的质量是_______ g,含 个分子,含______mol氧原子,该硫酸所含氢元素的质量与 mol HCl中所含氢元素的质量相同。
(2)在相同条件下,含有相同分子个数的SO2和SO3,其质量比为,物质的量比为,其中所含氧原子个数比为。
在标准状况下,1体积水溶解700体积氨气,所得溶液密度为0.9g/cm3,这种氨水的物质的量浓度和溶质的质量分数分别为
| A.18.4mol·L-1 34.7% | B.20.4mol·L-1 38.5% |
| C.18.4mol·L-1 38.5% | D.20.4mol·L-1 34.7% |