某化工厂技术员小李分析氯化钡和氯化钠组成的产品中氯化钠的质量分数,取16.25g固体样品全部溶于143.6g水中,向所得溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图表示的曲线关系。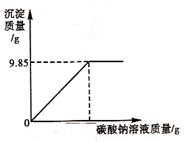
(1)当氯化钡与碳酸钠恰好完全反应时,消耗10.6%的碳酸钠溶液的质量是多少?
(2)产品中氯化钠的质量分数是多少?
(3)当氯化钡与碳酸钠恰好完全反应时,过滤所得溶液中溶质的质量分数是多少?
将104g由氯化钠和氯化钡
组成的固体混合物溶解于足量水中,向所得溶液中滴加10.6%的碳酸钠溶液,所加碳酸钠溶液的质量与生成沉淀质量关系见右图
①图中表示恰好完全反应的点是,此时溶液中的溶质为。(写化学式)
②求生成沉淀的质量。
③求原混合物中氯化钠的质量分数。

农技人员采用“测土配方”技术对一片果园进行了土壤检测,结果显示该果园需要补充一定量的氮元素和钾元素。
(1)、氮是植物生长的重要元素,果园土壤中缺少氮元素,需要用氮肥来补充,下列属于氮肥的是(填序号)。
①KCl;②NH4HCO3;③Ca3(PO4)2。
(2)、某同学取丰收牌钾肥(如上图)样品2.0g,溶于足量的水中,滴加过量氯化钡溶液,产生沉淀质量与所加氯化钡溶液质量的关系如右图。试通过计算判断该钾肥中硫酸钾的质量分数是否符合产品外包装说明?(反应方程式为:K2SO4+BaCl2=BaSO4↓+2KCl,杂质不参加反应。)
(1)医用生理盐水为0.9%的NaCl溶液。实验室现有下列药品:足够的蒸馏水、足够的NaCl、500g溶质喷量分数为1.5%的NaCl溶液、800g溶质质量分数为0.5%的NaCl溶液。现欲配制100g生理盐水.请你没计出两种配制方案并写出解答过程。(各溶液的密度都为1 g·cm-3)
(2)为了检验上述配制的生理盐水是否符合医用标准,某兴趣小组的同学取该生理盐水130g,向其中加入足量的AgNO3。溶液完全反应后,生成沉淀2.87g,通过计算判断该生理盐水是否符合医用标准。
某校兴趣小组在实验室中完成制取氧气的实验。他们取氯酸钾和二氧化锰的混合物共3.0g放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
| 反应时间/min |
1.0 |
1.5 |
2.0 |
2.5 |
3.0 |
3.5 |
| 剩余固体质量/g |
2.55 |
2.25 |
2.10 |
2.04 |
M |
2.04 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气的质量为_______________g;
(2)根据表中数据分析M的值是_g
(3)原混合物中氯酸钾的质量分数是多少?(请写出计算过程)
将一定质量的碳酸钠粉末溶于
克水中配制成溶液,取一半该溶液,向其中加入
的盐酸若干克,恰好反应完全,放出气体的质量为
克。试计算:
(1)碳酸钠溶液的总质量;
(2)反应后所得溶液中溶质的质量分数。