下列说法正确的是
A.按系统命名法,化合物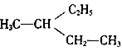 的名称为2-乙基丁烷 的名称为2-乙基丁烷 |
| B.甘油和甲苯只有在物质的量之比1︰1混合时,充分燃烧后生成的水,才与等质量的甘油充分燃烧后生成的水相同 |
| C.分子式为C5H10O2的酯类物质有9种 |
| D.不粘锅表面的高分子涂层可以由四氟乙烯通过缩聚反应合成 |
下列反应原理不符合工业冶炼金属实际情况的是
A.2HgO 2Hg+O2↑ 2Hg+O2↑ |
B.2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑ |
C.2MgO(熔融) 2Mg+O2↑ 2Mg+O2↑ |
D.Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
下列说法正确的是
| A.酸式盐的水溶液一定显酸性 |
| B.酸性氧化物一定是非金属氧化物 |
| C.丁达尔效应是溶液和胶体的本质区别 |
| D.HClO是弱酸,但NaClO是强电解质 |
下列变化中不属于化学变化的是
| A.紫色的石蕊试液中通入CO2后变色 | B.SO2漂白草编制品 |
| C.木炭使红棕色的NO2气体褪色 | D.淀粉遇碘变蓝色 |
化学与科技、环境、社会、生产生活密切相关,下列有关说法不正确的是
| A.绿色化学的核心是利用化学原理治理环境污染 |
| B.硅酸钠的水溶液俗称水玻璃,是制备硅胶和木材防火剂的原料 |
| C.大量使用风能、太阳能、生物质能,符合“低碳”理念 |
| D.蒙古牧民喜欢用银器盛放鲜牛奶有其科学道理:用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 |
在Na2CO3和HCl反应的下列各组实验中,反应速率最慢的一组是
| 组号 |
温度(℃) |
Na2CO3浓度(mol/L) |
HCl浓度(mol/L) |
| A |
10 |
0.1 |
0.2 |
| B |
20 |
0.2 |
0.2 |
| C |
10 |
0.2 |
0.4 |
| D |
20 |
0.2 |
0.4 |