常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.pH=12的溶液:NH4+、K+、SO42-、NO3- |
| B.澄清透明的溶液:Mg2+、Na+、SO42-、Br- |
| C.0.1 mol·L-1 Na2CO3溶液:NH4+、Ca2+、SO42-、NO3- |
| D.c(Fe3+)=0.1 mol·L-1溶液:H+、K+、Cl-、SCN- |
有一块铝铁合金,将其溶解于足量盐酸中,再加入过量NaOH溶液,在空气中静置至红褐色沉淀不再增加时,将沉淀滤出再灼烧至恒重,得到残留物的质量与原合金质量相同,则合金中铝的质量分数()
| A.52.4% | B.30% | C.70% | D.47.6% |
已知反应4HNO3(浓)+Cu=Cu(NO3)2+2NO2↑+2H2O,下列说法正确的是()
| A.HNO3是氧化剂,NO2是氧化产物 |
| B.若2mol HNO3(浓)完全反应,则反应中共转移了NA个电子 |
| C.还原剂与氧化剂的物质的量比是1 :4 |
| D.氧化产物和还原产物的物质的量之比为2 :1 |
下列各组中均为两瓶无标签的无色溶液,不许使用其它任何试剂(包括水),也能鉴别出来的是()
①NaOH和Al2(SO4)3②Na2CO3和盐酸③NaHCO3和盐酸④盐酸和NaAlO2
| A.①②③ | B.②③④ | C.①③④ | D.①②④ |
在某无色溶液中缓缓地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子是()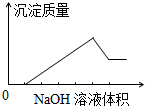
| A.Mg2+、Al3+、Fe2+ | B.H+、Mg2+、Al3+ | C.H+、Ba2+、Al3+ | D.只有Mg2+、Al3+ |
下列反应的离子方程式书写正确的是()
| A.稀盐酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
| B.水玻璃中通入过量二氧化碳气体:SiO32-+CO2+H2O=H2SiO3+CO32- |
| C.浓烧碱溶液中加入铝片:Al+OH-+H2O=AlO2-+H2↑ |
| D.NaHSO4与足量Ba(OH)2溶液混合:H+ + SO42-+ Ba2++ OH- =BaSO4↓+H2O |