(8分)为了鉴别碳酸钾溶液和氢氧化钾溶液,同学们进行了探究实验,分别取两种溶液于两支试管中,各滴入一定量的氯化钙溶液,观察到一支试管中出现白色浑浊,实验结束后,同学们将废液倒入同一个干净的烧杯中,发现废液变浑浊,同学们对废液进行了过滤,并对滤液的成分进行了探究.
【提出问题】滤液中除水外还含有那些物质?
【猜想】A.可能含有氢氧化钾、氯化钾和碳酸钾
B.可能含有氢氧化钾、氯化钾
C.可能含有氢氧化钾、氯化钾、碳酸钾和氯化钙
你认为还可能是 (写出一种猜想)
【讨论】你认为 猜想不合理(填字母),请说明理由 .
【实验设计】设计一个简单的实验,证明你的猜想正确.
| 实验步骤 |
实验现象 |
实验结论 |
| 取样于试管中, |
|
猜想正确 |
【反思交流】写出碳酸钾与氯化钙反应的化学方程式 ,在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑 .
用如图所示装置测定空气氧气的含量:在一个具有刻度和可以滑动的活塞的玻璃容器中放入一粒白磷(白磷燃烧所需的最低温度为40℃),将玻璃容器固定好,放在盛有85℃热水的烧杯上。请回答下列问题:
⑴实验中可以看到玻璃容器内白磷燃烧的现象是,该反应的化学(符号)表达式为。
⑵活塞在整个实验中的运动状况是先向,原因是;然后向,最后停在刻度_ ___处。
⑶玻璃容器内余下的气体主要是____,该实验能体现出该气体所具有的化学性质是、。
小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分。
[提出问题] 该淡黄色固体的化学成分是什么?
[查阅资料]
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
[设计实验方案]
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是,理由是(从环保、操作等角度分析)。
[实验验证并得出结论]
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH)。通过实验验证,确定该淡黄色粉末为过氧化钠。
小明想对生成的气体成分判断,他提出了以下两种假设:
①该气体是CO②该气体是O2
你认为上述假设哪个更合理?并说明选择的理由。 。
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论)。
| 操作步骤 |
实验现象 |
结论 |
[计算] 在过氧化钠(Na2O2)中,①氧元素的化合价为;
②过氧化钠中钠、氧元素的质量比为;
78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?(列式计算 )
请你根据提供的实验装置和药品,参与实验室气体制备的探究。
A B C D E F
【提供药品】高锰酸钾、稀盐酸、大理石
【熟悉仪器】请填写标号仪器的名称:①_________,②________。
【比较研究】根据所提供的药品,填写下表。
| 气体 |
反应物状态 |
反应条件 |
收集方法和依据 |
|
| 二氧化碳 |
固体和液体 |
常温 |
向上排空气法 |
CO2密度比空气大 |
| 氧气 |
固体 |
加热 |
排水法 |
①______________ |
| ②_____________ |
O2密度比空气略大 |
【实践研究】(1)用加热高锰酸钾的方法制取氧气,应选用发生装置A,写出该反应的文字表达式__________________________。
(2)下列是某同学用加热高锰酸钾制取氧气,并用排水法收集的部分实验操作,其中不合理的是___。
A.先检查装置的气密性,后加药品
B.先将导管伸入集气瓶,后加热试管
C.实验结束先将导管移出水面,后熄灭酒精灯
(3)实验室制取可用___装置组合(填字母编号)可制取二氧化碳,写出实验室制取二氧化碳的文字表达式____________________________________。
【反思小结】实验室制取气体的发生装置和收集装置的选择依据:
发生装置的选择依据——_________和_________。
收集装置的选择依据——气体的______、气体在水中的______,该气体能否与空气或水反应。【拓展应用】实验室用锌粒和稀硫酸反应制取氢气,应选用的发生装置是B或C, C与B相比较,其优点是_______________________;氢气是密度最小的气体,难溶于水,可选用的收集装置为___(填字母编号)。
某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成氮化镁(Mg3N2),设计了如下方案进行验证。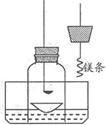
步骤l:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如图所示的装置;另准备一只有一根铜丝穿过的橡皮塞,
铜丝末端固定一根镁条。
步骤2:引燃燃烧匙中足量的红磷,塞好橡皮塞;待充分冷却,
观察到广口瓶内水面上升的体积约占瓶内水面原上方空间的1/5左右。
步骤3:往水槽中加水使广口瓶内外水面相平;点燃镁条,更换橡皮塞,镁条在广口瓶内继续燃烧,放出热量;待冷却后广口瓶内水位继续上升。
(1)步骤2的目的是。写出红磷在氧气中燃烧的化学方程式;
(2)在步骤3“待冷却后广口瓶内水位继续上升”是由于瓶内气压(选填“大于”“小于”或“等于”)外界气压。
(3)根据上述实验和你所学的知识,请写出镁在空气中燃烧时的化学方程式:①镁与氧气反应:;②①镁与氮气反应:。
某化学兴趣小组同学为了研究影响分子运动速率的因素,如下图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨水。浓氨水挥发出来的氨气(NH3)和浓盐酸挥发出来的氯化氢(HCl)能发生如下反应,NH3+ HCl=NH4Cl。两个注射器同时向脱脂棉靠]近里边的部位注入等体积的液体,过一会,先在A处产生大量白烟,然后白烟逐渐充满整个试管。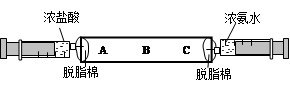
根据现象回答问题:
(1)生成物NH4Cl常温下的状态是(填“固体”、“液体”或“气体”);
(2)有同学认为先在A处产生白烟是因为HCl分子比NH3分子运动速度慢,请你分析影响分子运动速度的因素可能是;
(3)影响分子运动速率的因素还有温度,请举出生活中的一个实例;
(4)该实验中的注射器也可改用胶头滴管直接滴入液体,相比较用注射器的优点是 。