黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
| 样品 |
第1份 |
第2份 |
第3份 |
第4份 |
第5份 |
| 取样品质量(g) |
40.0 |
40.0 |
40.0 |
40.0 |
40.0 |
| 取稀硫酸质量(g) |
30.0 |
60.0 |
90.0 |
120.0 |
150.0 |
| 产生气体质量(g) |
0.3 |
0.6 |
0.9 |
1.0 |
1.0 |
按要求回答下列问题:
(1)根据实验数据分析,从第 份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)
(3)在给出的坐标纸上,画出40.0g样品中加稀硫酸的质量与产生气体质量的关系曲线。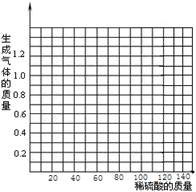
最近媒体报道油炸含有淀粉的食品会产生有毒的丙烯酰胺【 化学式为C3H5NO 】,食用后有害健康。试计算 (要求写出计算过程,写在第6页上,注意解题格式!) :
(1)丙烯酰胺的相对分子质量是多少?
(2)丙烯酰胺中各元素的质量比m(C) :m(H) :m(N) :m(O)是多少?
(3)丙烯酰胺中碳元素的质量分数是多少(计算结果精确至0.1%)?
(4)71g丙烯酰胺与多少克 CO2中所含碳元素的质量相等?
将0.5g二氧化锰与一定量氯酸钾共热到质量不减少为止,称得残渣质量为15.4g。求:(1)生成氧气多少克? (2)原氯酸钾的质量是多少克?
水果中含有柠檬酸,可促进消化。柠檬酸的化学式为C6H8O7
⑴柠檬酸的相对分子质量为__________;
⑵柠檬酸中的碳、氢、氧三种元素的质量比为(化成最简整数比)__________;
⑶柠檬酸中碳元素的质量分数是__________。
玛丁啉是一种常见的胃药,可促进胃动力,消除胃胀和胃痛等不适症状。已知玛丁啉的化学式为C22H24ClN5O2,请回答:
(1 ) 玛丁啉是由种元素组成的;
(2 ) 一个玛丁啉分子中共有个原子;
(3 ) 计算玛丁啉分子中N元素的质量分数(保留2位小数)。
锌是人体生长发育、维持器官正常功能的微量元素,人体缺锌会引起多种疾病,缺锌者可通过服用葡萄糖酸锌口服液等保健品来补锌。已知葡萄糖酸锌的化学式为C12H22O14Zn,请回答:
(1)标签上所标示的“每支口服液含锌为……”中的锌指的是()
A、锌原子 B、锌单质 C、锌元素 D、锌离子
(2)葡萄糖酸锌是由种元素组成,它的相对分子质量为,葡萄糖酸锌分子中C、H、O、Zn的原子个数比为。
(3)葡萄糖酸锌中锌元素的质量分数为多少?(结果保留至0.1%)
(4)现有一支葡萄糖酸锌口服液,其中含锌6.5mg,那么该口服液中葡萄糖酸锌的质量是多少?