本题为《化学与生活(选修1)》模块选做题,每空2分,共20分。
人类的衣食住行都离不开化学,化学与生活密切相关。
(1)根据要求,选择恰当的选项用字母代号填空:
①“含氟牙膏”中的氟应理解为 。
A.单质 B.元素 C.离子
②为适应低碳生活,上学或上班最好 。
A.乘私家车 B.乘公交车
③糖类、油脂、蛋白质、无机盐、水、维生素是人类不可缺乏的营养物质。
下列维生素中,可用于防治坏血病的是 。
A.维生素A B.维生素B1 C.维生素C
④抗生素药有阻止多种细菌生长的功能,下列药物属于抗生素药的是 。
A.阿司匹林 B.青霉素 C.抗酸药(氢氧化铝)
⑤下列方法不属于目前常用的垃圾处理方法的是 。
A.焚烧法 B.干馏法 C.堆肥法
(2)在全球每年被腐蚀的钢铁中,电化学腐蚀比化学腐蚀所占比例 (填“高”或“低”)。
(3)下表所列的一些物质都是家庭常用物质,请根据实验要求,选择合适的化学试剂,将其字母代号填入对应的空格中。
| 实验要求 |
化学试剂 |
供选择的化学试剂 |
| 检验味精中是否含有食盐 |
|
A.新制氢氧化铜悬浊液 B.硝酸银溶液和稀硝酸 C.碘水 D.碳酸钠粉末 |
| 检验地瓜粉中是否含有淀粉 |
|
|
| 检验食醋中是否含有乙酸 |
|
|
| 区别蔗糖和葡萄糖 |
|
工业上常常利用反应①来生产环氧乙烷,但是伴随副反应②。
①C2H4(g)+ O2(g) →
O2(g) →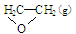 ;△H1②C2H4(g)+3O2(g) → 2CO2(g)+2H2O(g);△H2
;△H1②C2H4(g)+3O2(g) → 2CO2(g)+2H2O(g);△H2
(1)写出环氧乙烷充分燃烧的热化学反应方程式。答:____________________________;
(2)工业生产中,可通过某一措施来加快反应①而对反应②影响较小,从而提高环氧乙烷的生产效率。工业生产采取的这种措施是_______________。
A.升高反应体系的温度B.增大体系中氧气的浓度
C.使用合适的催化剂D.降低反应体系的压强
(3)已知C=C、O=O、C—C键能分别为a kJ·mol-1、b kJ·mol-1、c kJ·mol-1,则环氧乙烷中C—O键能为kJ·mol-1;
(4)反应②可以设计成燃料电池,若以酸做电解质溶液,负极反应式是。
在确定苯的结构的研究过程中,曾经有下列结构:a. 、b.
、b. 。
。
请回答下列问题:
(1)若苯的结构为a,则它与 结构在下列哪些方面不同 (填字母代号)。
结构在下列哪些方面不同 (填字母代号)。
| A.一氯代物的种类 | B.二氯代物的种类 |
| C.与溴水作用 | D.与氢气作用 |
(2)请设计一个实验证明上述b分子的结构简式不能表示苯的结构(要求写出简要的实验步骤)。
写出相应烷烃的分子式:
(1)同温同压下蒸气的密度是H236倍的烷烃 。
(2)分子中含有200个氢原子的烷烃 。
(3)1 L烷烃的蒸气完全燃烧时,生成同温同压下的水蒸气15 L 。
(4)分子中含有22个共价键的烷烃 。
下列各组物质中全属于有机物的是 ;全属于烃的是 。
| A.CH4、C2H5OH、C6H12O6(果糖)、(C6H10O5)n(淀粉) |
| B.C2H2、H2O2、CCl4、C6H6 |
| C.CH4、C2H4、H2CO3、CH3Cl |
| D.CH4、C2H6、C2H2、C6H6 |
将等物质的量的A、B、C、D四种物质混合放入V L密闭容器中,发生如下反应:aA+bB cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol。此时反应达到平衡。
cC(s)+dD,当反应进行到第t min时,测得A减少了n mol,B减少了n/2 mol,C增加了3n/2 mol,D增加了n mol。此时反应达到平衡。
(1)该化学方程式中,各物质的化学计量数分别为:a= ,b= ,c= ,d= 。
(2)以B的浓度变化表示的该化学反应的速率为v(B)= 。