【化学—选修2化学与技术】氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程图如下: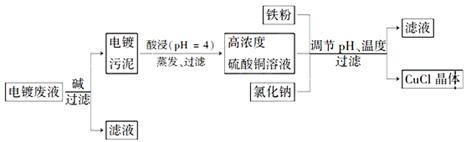
金属离子含量与混合液pH、CuCl产率与混合液pH的关系图如图。
【已知:金属离子浓度为1 mol·L-1时,Fe(OH)3开始沉淀和沉淀完全的pH分别为1.4和3.0,Cu(OH)2开始沉淀和沉淀完全的pH分别为4.2和6.7】
请回答下列问题:
(1)酸浸时发生反应的离子方程式是______;析出CuCl晶体时的最佳pH在_______左右。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为________________。
(3)析出的CuCl晶体要立即用无水乙醇洗涤,在真空干燥机内于70℃干燥2 h、冷却密封包装。70℃真空干燥、密封包装的目的是_____________________________________。
(4)产品滤出时所得滤液的主要分成是________,若想从滤液中获取FeSO4·7H2O晶体,还需要知道的是__________________。
(5)若将铁粉换成亚硫酸钠也可得到氯化亚铜,试写出该反应的化学方程式:_________________。为提高CuCl的产率,常在该反应体系中加入稀碱溶液,调节pH至3.5。这样做的目的是_____________。
1996年诺贝尔化学奖授予对发现 C60有重大贡献的三位科学家。C60分子是形如球状的多面体,如右图,该结构的建立基于以下考虑:C60分子中每个碳原子只跟相邻的3个碳原子形成化学键;C60分子只含有五边形和六边形;碳与碳之间既有单键又有双键,每个碳原子仍然满足四个价键饱和.
多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:
顶点数 + 面数 - 棱边数 =" 2" 。
请回答:
(1)一个C60分子中有多少个五边形和多少个六边形?
(2)一个C60分子中有多少个C=C?
(3)已知C70分子的结构模型也遵循C60的那些规律,请确定C70分子结构中上述几项参数。
试用杂化轨道理论分析为什么BF3的空间构型是平面三角形,而NF3是三角锥形的?
你认为水的哪些物理性质与氢键有关?试把你的结论与同学讨论交流。
乙醇(C2H5OH)和甲醚(CH3OCH3)的化学组成均为C2H6O,但乙醇的沸点为78.5℃,而甲醚的沸点为-23℃,为何原因?
据报道,2003年3月27日巨大的SO2、NO等排放量使广东成为酸雨的重灾区,占全省国土面积63%的17个城市已被国务院划为酸雨控制区,酸雨使大片水稻突然枯死,并且每年因酸雨污染造成的经济损失就达40亿元左右,问:
(1)酸雨导致水稻死亡的原因是什么?
(2)试简叙述酸雨的形成过程,并写出反应方程式。
(3)请提出两条防治酸雨的措施。