某温度下,体积和pH都相同的稀硫酸和硫酸铝溶液加水稀释时的pH变化曲线如图,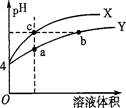
下列有关说法正确的是
| A.加等量的水后硫酸中水电离出的C(H+)与硫酸铝中水电离出的C(H+)的比值比稀释前的比值增大 |
| B.a点溶液中有:c(H+)+c(Al3+)=c(OH-)+c(SO42一) |
| C.体积和pH都相同的稀硫酸和硫酸铝溶液与等浓度的NaOH反应,消耗NaOH的体积相等 |
| D.b、c两溶液水电离出的c(OH-)相等。 |
事实上,许多非金属氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2 +SO2 = Na2SO4 2Na2O2 +2SO3= 2Na2SO4 +O2据此,你认为下列反应方程式中正确的是
| A.2Na2O2 + 2N2O4= 4NaNO3 |
| B.Na2O2 + 2NO2 = 2NaNO2 + O2 |
| C.2Na2O2 + 2N2O3= 4NaNO2 + O2 |
| D.2Na2O2 + 2 Mn2O7 = 4Na2MnO4 + O2 |
0.03mol铜完全溶于硝酸,产生氮的氧化物(NO、NO2、N2O4)混合气体共0.05mol。该混合气体的平均相对分子质量可能是
| A.30 | B.46 | C.66 | D.69 |
下列表示对应化学反应的离子方程式正确的是
| A.向稀HNO3中滴加Na2SO3溶液:SO32-+2H+ = SO2↑+ H2O |
| B.向Na2SiO3溶液中通入过量SO2:SiO32-+SO2 +H2O = H2SiO3↓+SO32- |
| C.Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
| D.向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O="4" Na++2Cu(OH)2↓+O2↑ |
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
| 操作 |
现象 |
结论 |
|
| A |
滴加BaC12溶液,再滴加盐酸 |
生成白色沉淀 |
原溶液中有SO42- |
| B |
用洁净铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
原溶液中有Na+无K+ |
| C |
滴加氯水和CC14,振荡、静置 |
下层溶液显紫色 |
原溶液中有I- |
| D |
滴加几滴稀NaOH溶液,将湿润红色石蕊试纸置于试管口 |
试纸不变蓝 |
原溶液中无NH4+ |
某实验小组对一含有Al3+的未知溶液进行了如下分析:(1)滴入少量氢氧化钠,无明显变化;(2)继续滴加NaOH溶液,有白色沉淀;(3)滴入过量的氢氧化钠,白色沉淀明显减少。实验小组经定量分析,得出如图所示沉淀与滴入氢氧化钠体积的关系。下列说法错误的是
| A.该未知溶液中至少含有3种阳离子 |
| B.滴加的NaOH溶液的物质的量浓度为5 mol·L-1 |
| C.若另一种离子为二价阳离子,则a=10 |
| D.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6 g |