能正确表示下列反应的离子方程式
| A.向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O―→2C6H5OH+CO32- |
| B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ |
| C.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+ |
| D.NaHCO3溶液与稀H2SO4反应:CO32-+ 2H+ = H2O + CO2↑ |
为提纯下列物质(括号内为杂质)选用的试剂和分离方法都正确的是
| 物质 |
试剂 |
分离方法 |
|
| ① |
硝酸钾(氯化钠) |
蒸馏水 |
降温结晶 |
| ② |
二氧化碳(氯化氢) |
饱和碳酸钠溶液 |
洗气 |
| ③ |
乙酸乙酯(乙酸) |
氢氧化钠溶液 |
分液 |
| ④ |
氯气(氯化氢) |
饱和氯化钠溶液 |
洗气 |
A.①③B.①④C.只有②D.③④
下列有关物质转化的叙述不正确的是
| A.SiO2→H2SiO3、CuO→Cu(OH)2、CuSO4→CuCl2均不能通过一步反应实现 |
| B.FeS、FeCl2、Fe(OH)3均可以通过化合反应制得 |
| C.水在化学反应中可能只做氧化剂、或只做还原剂、或既不做氧化剂也不做还原剂、或既做氧化剂又做还原剂 |
| D.在某一复分解反应中,也有可能弱酸是反应物,而强酸是生成物 |
在水溶液中,YO3n 和S2
和S2 发生如下反应:YO3n
发生如下反应:YO3n +3S2
+3S2 +6H+=Y
+6H+=Y +3S↓+3H2O,则YO3n
+3S↓+3H2O,则YO3n 中Y元素的化合价和原子最外层电子数分别为
中Y元素的化合价和原子最外层电子数分别为
| A.+4、6 | B.+7、7 | C.+5、7 | D.+5、5 |
下列离子方程式正确的是
| A.向CaCl2溶液中通入CO2:Ca2++CO2+H2O=CaCO3↓+2H+ |
B.漂白粉溶液中通入过量SO2:ClOˉ+H2O+SO2=HSO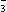 +HClO +HClO |
| C.在FeSO4溶液中加入H2O2溶液:Fe2++2H2O2+4H+=Fe3++4H2O |
D.在澄清石灰水中加入少量小苏打溶液:Ca2++OHˉ+HCO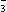 =CaCO3↓+H2O =CaCO3↓+H2O |
在200mL含Mg2+、Al3+、NH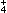 、H+、Clˉ等离子的溶液中,逐滴加入5mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如下图所示。下列叙述正确的是
、H+、Clˉ等离子的溶液中,逐滴加入5mol/L的NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)的关系如下图所示。下列叙述正确的是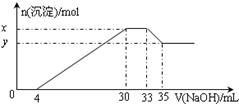
| A.原溶液中n(Mg2+)∶n(Al3+)=5∶2 |
| B.原溶液的pH=2 |
| C.x与y的差值为0.01mol |
| D.原溶液中c(Clˉ)=0.75mol/L |