某混合溶液中可能含有下列离子中的若干种:NH4+、Na+、Al3+、Fe2+、Fe3+、AlO2-、SO42-、I-、NO3-、CO32-,已知各离子的浓度均约为0.1mol/L,现取两份20mL该溶液进行如下实验:(1)第一份加入足量盐酸,产生气体在空气中变为红色,在反应后的溶液中加入BaCl2溶液,有白色沉淀产生。(2)第二份逐滴滴加NaOH溶液至过量,产生沉淀但不溶解,并有气体逸出。根据上述实验情况,以下说法错误的是
| A.该混合溶液中一定不含有Fe3+、AlO2-、Al3+、CO32- |
| B.该混合溶液通过继续进行焰色反应可以间接确定是否含有I- |
| C.该混合溶液中肯定含有Fe2+、NH4+、SO42-、NO3- |
| D.向该混合溶液中滴加酚酞试液后呈红色 |
一定温度下,将1 mol A和1 mol B气体充入2L恒容密闭容器,发生反应A(g)+B(g)  xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确是
| A.反应方程式中的x=l |
| B.t2时刻改变的条件是使用催化剂 |
| C.t3时刻改变的条件是移去少量物质D |
| D.t1~t3间该反应的平衡常数均为4 |
下图所示装置I是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为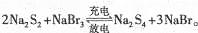 闭合开关K时,b极附近先变红色。下列说法正确的是
闭合开关K时,b极附近先变红色。下列说法正确的是
| A.当有0.01 mol Na+通过离子交换膜时,b电极上析出112 mL的气体 |
| B.负极反应为3Br--2e-= Br3- |
| C.闭合K后,b电极附近的pH变小 |
| D.闭合K后.a电极上有氯气产生 |
用下图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是
| 选项 |
甲 |
乙 |
丙 |
试管中现象 |
| A |
浓盐酸 |
二氧化锰 |
石蕊溶液 |
先变红后褪色 |
| B |
浓氨水 |
生石灰 |
A1Cl3溶液 |
先沉淀后消失 |
| C |
醋酸 |
碳酸钙 |
BaC12溶液 |
变浑浊 |
| D |
浓硝酸 |
铜 |
水 |
试管口出现红棕色 |
下列各组离子能大量共存,向溶液中通入足量相应气体后,各离子还能大量存在的是
| A.氯气:K+、Ba2+、SiO32-、NO3- |
| B.二氧化硫:Na+、NH4+、SO32-、C1- |
| C.氨气:K+、Na+、AlO2-、CO32- |
| D.甲醛:Ca2+、Mg2+、MnO4-、NO3- |
去年下半年我省雾霾天气十分严重。PM2.5细颗粒物含有的毒性物质来源之一是汽车尾气排放。通过排气管加装催化装置,可有效减少CO和NO的排放,催化装置内发生的反应为:NOx+CO—催化剂→N2+CO2,下列关于此反应的说法中,不正确的是
| A.所涉及元素的第一电离能:N>O>C |
| B.当x=2时,每生成1molN2,转移电子数为4mol |
C.等物质的量N2和CO2中, 键的个数比为1:1 键的个数比为1:1 |
| D.氧化剂与还原剂的物质的量之比为1:1时,NOx中氮元素的化合价为+2价 |