短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是
| A.离子半径:r(Y2-)>r(Z2+) |
| B.Y分别与Z、W形成的化合物中化学键类型相同 |
| C.Y的气态简单氢化物的热稳定性比氮元素的气态简单氢化物弱 |
| D.X、Y、Z、W所有元素的最高正价等于其所在族的族序数 |
随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。下列有关说法中正确的是 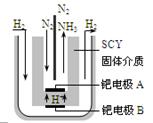
| A.电解法合成氨的电解池中能用水作电解质溶液的溶剂 |
| B.钯电极B连接的是电源的负极 |
| C.钯电极A的电极反应式为:N2+6e—+6H+==2NH3 |
| D.当有0.3mol电子转移时,有2.688L NH3生成 |
下列反应中,氧化剂与还原剂物质的量的关系为1:2的是
| A.4KI+O2+2H2O=4KOH+2I2 |
| B.2CH3COOH+Ca(ClO)2=2HClO+(CH3COO)2 Ca |
| C.I2+2NaClO3=2NaIO3+Cl2 |
D.MnO2+4HCl MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
某实验小组依据反应 设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
A.调节pH可以改变反应的方向
B.pH = 0.68时,反应处于平衡状态
C.pH = 5时,负极电极反应式为2I--2e- =I2
D.pH >0.68时,氧化性I2〉AsO43-
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族。a的原子结构示意图为 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为 ,下列比较中正确的是( )
,下列比较中正确的是( )
| A.原子半径:a>c>d>b | B.最高价氧化物对应水化物的酸性:c>d>a |
| C.原子序数:a>d>b>c | D.单质的氧化性:a>b>d>c |
下列说法不正确的是
| A. |
B. |
C. |
D. |
| 通电一段时间后,搅拌均匀,溶液的pH增大 |
甲电极上的电极反应为: 2Cl- -2e- = Cl2↑ |
Pt电极上的电极反应为:O2+2H2O+4e-==4OH- |
总反应的离子方程式为: 2Fe3++Cu=Cu2++ 2Fe2+ |
 |
 |
 |
 |